
| 温度(℃) 平衡态 | 260 | 270 | 280 | 290 | 300 | 310 |
| CO转化率(%) | 92 | 87 | 82 | 80 | 72 | 62 |
| CH3OCH3产率(%) | 33 | 45 | 77 | 79 | 62 | 52 |
| A. | 反应①、②均为吸热反应 | |
| B. | 290℃时反应②K值达到最大 | |
| C. | 平衡时,反应①与②中CH3OH的消耗速率一定相等 | |
| D. | 增大压强能增大CH3OCH3产率 |
分析 A.CO的转化率随温度升高而降低,说明升高温度反应①平衡逆向移动,甲醚的产率开始随温度升高而增大,说明升高温度反应②向正反应移动;
B.反应②为吸热反应,升高温度平衡正向移动,温度越高平衡常数越大;
C.甲醇处于2个不同的反应体系,不能确定反应速率问题;
D.增大压强,不影响反应②的平衡移动,但反应①向正反应移动,甲醇浓度增大,使反应②正向移动.
解答 解:A.CO的转化率随温度升高而降低,说明升高温度反应①平衡逆向移动,正反应为放热反应,甲醚的产率开始随温度升高而增大,说明升高温度反应②向正反应移动,正反应为吸热反应,故A错误;
B.反应②为吸热反应,升高温度平衡正向移动,温度越高平衡常数越大,290℃时反应②K值不是最大,而温度高时甲醚产率减小,是由反应①逆向移动,甲醇浓度减小所致,①起主导作用,故B错误;
C.甲醇处于2个不同的反应体系,不能确定反应速率问题,故C错误;
D.增大压强,虽然不影响反应②的平衡移动,反应①为气体体积减小的反应,增大压强平衡正向移动,甲醇的浓度增大,使反应②正向移动,增大CH3OCH3产率,故D正确,
故选:D.
点评 本题考查化学平衡计算与影响因素,注意容器内2个关联的平衡体系相互影响,侧重考查学生分析能力,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol甲基所含有的电子数为10NA | |
| B. | 标准状况下,11.2L氯仿(CHCl3)中含有C-Cl键的数目为1.5NA | |
| C. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2 NA | |
| D. | 6.0g冰醋酸与4.6g乙醇反应生成乙酸乙酯的分子数为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
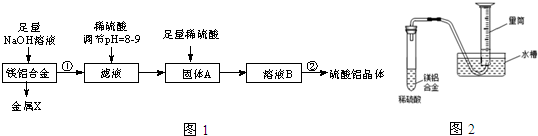
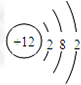 ,固体A的化学式为Al(OH)3;
,固体A的化学式为Al(OH)3;查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液:c(NH4+)大小顺序为①>②>③ | |
| B. | 0.l mol•L-1CuSO4•(NH4)2SO4•6H2O溶液:c(SO42-)>c(NH4+)>c(Cu2+)>c(OH-)>c(H+) | |
| C. | 0.1 mol•L-1Na2CO3溶液:C(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| D. | 等体积、等物质的量浓度的CH3COONa和CH3COOH混合后的溶液:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com