
分析 (2)分度盘的指针偏右,说明右边重,将左边的横梁螺丝往外调调节平衡;根据使用托盘天平时,加砝码的正确操作完成;
(3)该同学漏掉洗涤操作,导致部分溶质损耗,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(2)分度盘的指针偏右,说明右边重,左盘高于右盘.应将将左边的平衡螺母左旋移动,或将右边的平衡螺母左旋,直至天平平衡;
故答案为:高于;将左边的平衡螺母左旋移动,或将右边的平衡螺母左旋,直至天平平衡;
(3)该同学漏掉洗涤操作,导致部分溶质损耗,依据C=$\frac{n}{V}$可知溶液浓度偏低;
故答案为:偏低.
点评 本题以一定物质的量浓度溶液的配制为载体考查了托盘天平的使用方法和溶液配制误差分析的方法,熟悉托盘天平工作原理、明确不当操作对溶质的物质的量和溶液体积的影响是解题关键,题目难度不大.


 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源:2016-2017学年陕西西藏民族学院附中高二上月考二化学卷(解析版) 题型:选择题
下列各变化中不属于原电池的反应的是( )
A.为防止轮船外壳生锈,在船底装上锌块
B.镀锌铁表面锌有划损时,也能阻止铁被氧化
C.在空气中金属铝表面迅速氧化形成保护层
D.锌和稀硫酸反应时,加入少量的CuSO4溶液可使反应加快
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NH4HCO3溶液中加入少量的Ba(OH)2溶液并加热:Ba2++2OH-+NH4++HCO3-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+2H2O+BaCO3↓ | |
| B. | 电解氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 少量CO2通入苯酚钠溶液:2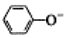 +CO2+H2O→2 +CO2+H2O→2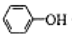 +CO32- +CO32- | |
| D. | 向明矾溶液中滴加Ba(OH)2溶液至溶液呈中性:2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸中的HNO3见光会分解,因此有时在实验室看到的浓硝酸呈黄色 | |
| B. | SO2具有漂白性,因此可使溴水褪色 | |
| C. | Na的金属性比Cu强,因此可用Na与CuSO4溶液反应制取Cu | |
| D. | Fe在Cl2中燃烧生成FeCl3,因此在与其他非金属反应的产物中Fe也显+3价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “雨后彩虹”是与胶体、光学等知识有关的自然现象 | |
| B. | “百炼成钢”主要发生了物理变化 | |
| C. | “返青粽叶”指的是添加胆矾(CuSO4•5H2O)后的粽叶青绿新鲜,长期食用有害健康,其中胆矾是混合物 | |
| D. | “明矾净水”与漂白粉用于自来水消毒的原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
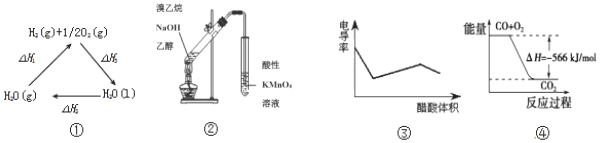
| A. | 图①中△H1=△H2+△H3 | |
| B. | 图②可用于证明实验中生成了乙烯 | |
| C. | 图③表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲线 | |
| D. | 图④可表示由CO(g)生成CO2(g)的过程中要放出566kJ 热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com