
下列关于碳酸氢钠的分类不正确的是
A.钠盐 B.含氧酸盐 C.化合物 D.碱
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源:2014-2015学年安徽省江南十校高三上学期期末联考理综化学试卷(解析版) 题型:填空题
(16分)聚乙酸乙烯酪广泛用于制备涂料、粘合剂等,它和高聚物长的合成路线如下:
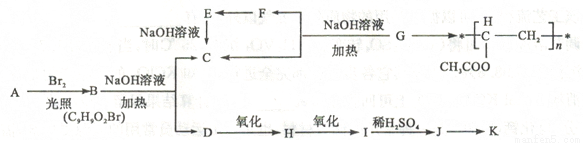
其中J物质与氯化铁溶液能发生显色反应,且苯环上的一元取代物原有两种。
已知①当羟基与双键碳原子相连时,易发生如下转化RCH =CHOH→RCH2CHO
②一ONa连在烃基生不会被氧化
请回答下列问题:CH3COO CH3 CH2Br
(1)写出G的结构简式 。F与H中具有相同官能团的名称 。
(2)上述变化中G→C+F 的反应类型是 ;J在一定条件下能生成高聚物K,K的结构简式是 。
(3)写出B→C+D反应的化学方程式: 。
(4)同时符合下列要求的A的同分异构体有 种。
I含有苯环
II能发生银镜反应和水解反应
并写出满足下列条件的同分异构体结构简式: 。
①核磁共振氢谱有5 个吸收峰
②1mol该同分异构体能与Imol NaOH 反应
(5)下列有关说法正确的是 。
a.1 mol A 完全燃烧消耗10.5 mol O2
b.J与足量的碳酸氢钠溶液反应能生成相应的二钠盐
c.D→H 的试剂通常是KMO4 酸性溶液
d.J能发生加成、消去、取代、氧化等反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高三上学期期末考试化学试卷(解析版) 题型:选择题
能用溴水鉴别的是
A.甲烷、乙烯 B.甲烷、乙烷
C.NaCl溶液、KCl溶液 D.MgSO4溶液、Mg(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源:2015年湖北省荆门市高三元月调考理综化学试卷(解析版) 题型:实验题
(14分)肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4·H2O)。CO(NH2) + 2NaOH + NaClO = Na2CO3 + N2H4·H2O + NaCl
实验一:制备NaClO溶液
(1)将氯气通入到盛有NaOH的锥形瓶中,锥形瓶中发生反应的离子方程式是 ;
实验二:制取水合肼(实验装置如图所示)

控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分。(已知:N2H4·H2O + 2NaClO=N2↑ + 3H2O + 2NaCl)
(2)分液漏斗中的溶液是 (填标号A或B);
A.NaOH和NaClO混合溶液
B.CO (NH2) 2溶液
选择的理由是 ;
实验三:测定馏分中肼含量水合肼具有还原性,可以生成氮气。测定水合肼的质量分数可采用下列步骤:
a.称取馏分5.000g,加入适量NaHCO3固体,经稀释、转移、定容等步骤,配制250mL溶液。
b.移取25.00 mL于锥形瓶中,加入10mL水,摇匀.
c.用0.2000mol/L碘溶液滴定至溶液出现微黄色且半分钟内不消失,滴定过程中,溶液的pH保持在6.5左右。记录消耗碘的标准液的体积。
d.进一步操作与数据处理
(3)水合肼与碘溶液反应的化学方程式 ;滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是 。
(4)滴定时,碘的标准溶液盛放在 滴定管中(选填:“酸式”或“碱式”);若本次滴定消耗碘的标准溶液为18.00mL,馏分中水合肼(N2H4·H2O)的质量分数为 (保留三位有效数字);
(5)为获得更可靠的滴定结果,步骤d中进一步操作主要是: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市七校高三上学期期末联考理综化学试卷 (解析版) 题型:选择题
设NA表示阿伏加德罗常数,下列说法正确的是
A.标准状况下,22.4 L水所含电子数约为10 NA
B.25℃时,pH=13的1 L Ca(OH)2溶液中含有OH-数目约为0.2 NA
C.0.5 mol NH4HSO4晶体中,含有H+数目约为0.5 NA
D.常温常压下,3.2 g O2和O3混合气体含有0.2 NA个氧原子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省杭州地区7校高三上学期期末模拟联考化学试卷(解析版) 题型:实验题
(8分)溴化钙可用作阻燃剂、制冷剂,具有易溶于水,易吸潮等性质。实验室用工业大理石(含有少量Al3+、Fe3+等杂质)制备溴化钙的主要流程如下:
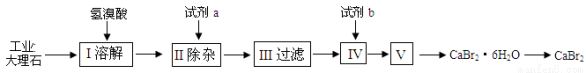
完成下列填空:
(1)上述使用的氢溴酸的质量分数为26%,若用47%的氢溴酸配置26%的氢溴酸的HBr 500ml,所需的玻璃仪器有玻璃棒、烧杯、量筒、 、 。
(2)已知步骤Ⅲ的滤液中不含NH4+。步骤Ⅱ加入的试剂a是 ,控制溶液的pH约为8.0的目的是 。步骤Ⅳ的目的是 。
(3)制得的溴化钙可以通过如下步骤测定其纯度:
①称取4.00g无水溴化钙样品;②溶解;③滴入足量Na2CO3溶液,充分反应后过滤、洗涤、干燥、称量。若得到1.88g碳酸钙,则溴化钙的质量分数为 (保留两位小数)。
②若实验操作规范而测定结果偏低,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com