
| A | B | C | D |
 |  |  |  |
| 陶瓷的烧制 | 活字印刷排版术 | 鞭炮和烟火的燃放 | 司母戊鼎表面出现铜绿 |
| A. | A | B. | B | C. | C | D. | D |
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
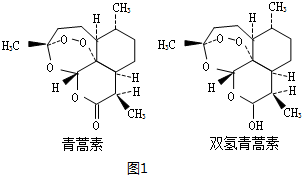
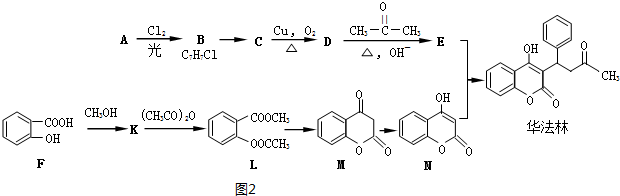
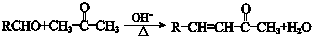
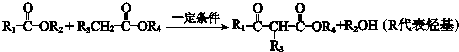
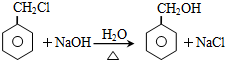 ;
;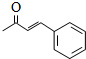 .L→M的转化中,会产生少量链状高分子聚合物,该聚合物的结构简式为
.L→M的转化中,会产生少量链状高分子聚合物,该聚合物的结构简式为 .
.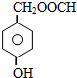 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色 | |
| B. | 烃与卤素单质之间的反应均为加成反应 | |
| C. | 多糖、油脂均可发生水解反应 | |
| D. | 石油分馏和裂化均为物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
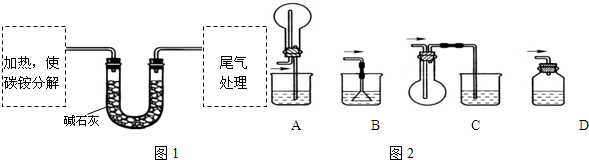
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
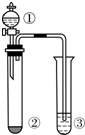 下表所列实验探究,利用如图所示实验装置,能得出相应实验结论的是( )
下表所列实验探究,利用如图所示实验装置,能得出相应实验结论的是( )| 选项 | ① | ② | ③ | 实验结论 |
| A | 水 | 电石 | CuSO4溶液 | 乙炔具有还原性 |
| B | 浓硝酸 | Cu | KI-淀粉溶液 | 氧化性:NO2>KI |
| C | 浓盐酸 | KMnO4 | KI-淀粉溶液 | 氧化性:KMnO4>Cl2>I2 |
| D | 稀硫酸 | Na2S | AgNO3与AgCl的浊液 | 溶解度:AgCl>Ag2S |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| m | n | ||
| x | y |
| A. | x最高价氧化对应水化物的碱性比y弱 | |
| B. | m可形成多种氢化物,而n只形成一种氢化物 | |
| C. | x的单质在m的最高价氧化物中燃烧,生成两种固体物质 | |
| D. | m、n两元素所形成的化合物分子中,既含有离子键,也含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
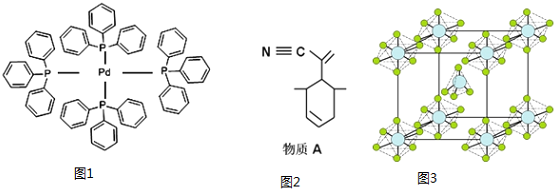
 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com