
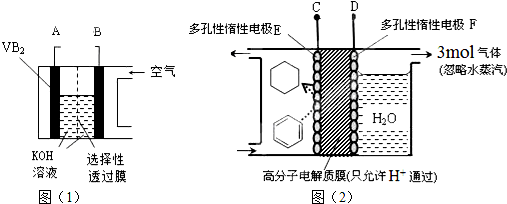
| A. | 整套装置工作时的连接为A连接D、B连接C | |
| B. | VB2极发生的电极反应为:2VB2+22OH--22e-═V2O5+2B2O3+11H2O | |
| C. | 电极F产生3mol气体时电极E得到的氧化产物为2mol | |
| D. | 储氢装置工作时,右侧电极区的pH值减小2×10-9 |
分析 硼化钒-空气燃料电池中,VB2在负极失电子,所以A是负极,氧气在正极上得电子,B是正极,电池总反应为:4VB2+11O2═4B2O3+2V2O5;硼化钒(VB2)-空气电池为电源给图(2)所示装置通电,根据图知,苯中的碳得电子生成环己烷,则E作阴极,F作阳极,阳极和电源正极相连,阴极和电源的负极相连,据此回答.
解答 解:A、硼化钒-空气燃料电池中,A是负极,B是正极,E作阴极,F作阳极,阳极和电源正极相连,阴极和电源的负极相连,整套装置工作时的连接为A连接C、B连接D,故A错误;
B、负极上是VB2失电子发生氧化反应,则VB2极发生的电极反应为:2VB2+22OH--22e-=V2O5+2B2O3+11H2O,故B正确;
C、F作阳极,阳极上氢氧根离子放电生成氧气,阳极上生成3mol氧气,转移电子的物质的量=3mol×4=12mol,电极E阴极上苯得电子和氢离子生成环己烷,电极反应式为C6H6+6H++6e-=C6H12,转移电子3mol,得到0.5molC6H12,故C错误;
D、储氢装置工作时,右侧电极是阳极区,氢氧根离子放电生成氧气,该电极区反应为:4OH--4e-=O2+2H2O,该电极区的pH值减小,当生成3mol氧气时,产生3mol氢离子,但是无溶液体积,不能计算,故D错误.
故选B.
点评 本题考查了原电池和电解池原理应用等知识点,根据电极反应是即可解答,注意知识的迁移应用是关键,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 温度越高,酶的催化活性越强 | |
| B. | 浓硝酸使皮肤呈黄色是由于浓硝酸与蛋白质发生了显色反应 | |
| C. | 用灼烧的方法可以鉴别毛织物和棉织物 | |
| D. | 在豆浆中加入少量的石膏,能使豆浆凝结为豆腐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鉴定蔗糖水解产物中有葡萄糖:在水解液中直接加入新制Cu(OH)2悬浊液 | |
| B. | 鉴别织物成分是真丝还是人造丝:灼烧 | |
| C. | 鉴定苯中有无碳碳双键:加入高锰酸钾酸性溶液 | |
| D. | 鉴别乙烯和乙烷:分别通入高锰酸钾酸性溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
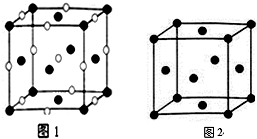
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
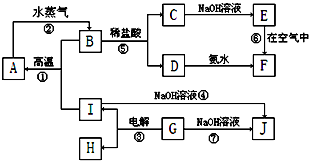
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气与水反应:Cl2+H2O?2H++Cl-+ClO- | |
| B. | 碳酸钡溶于醋酸:BaCO3+2H+═Ba2++H2O+CO2↑ | |
| C. | 金属钠跟水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 澄清石灰中通入过量二氧化碳:Ca2++2OH-+CO2═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com