
| A. | H2O(g)=H2O(l)△H=-44kJ/mol,所以该过程是放热反应 | |
| B. | 人类利用的能源都是通过化学反应获得的 | |
| C. | 2CO(g)+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2(g)△H<0,则56gCO和32gO2所具有的总能里大于88g所具有的总能量 | |
| D. | 需要加热的反应一定是吸热反应 |
分析 A.气态水变为液态水是物理变化,不能称为放热反应;
B.人类利用的能源不都是通过化学反应获得的;
C.放热反应,反应物的总能量大于生成物的总能量;
D.需要加热的反应可能是放热反应.
解答 解:A.气态水变为液态水是物理变化,可称为放热过程,不能称为放热反应,故A错误;
B.人类利用的能源不都是通过化学反应获得的,如风能等,故B错误;
C.2CO(g)+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2(g)△H<0,是放热反应,反应物的总能量大于生成物的总能量,故C正确;
D.需要加热的反应可能是放热反应,如可燃物的燃烧,故D错误;
故选C.
点评 本题考查吸热反应和放热反应,难度不大,注意吸热反应和放热反应是针对化学反应而言的,与反应的条件没有必然联系.


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,100mLPH=1的CH3COOH溶液中含有的H+总数大于0.01NA | |
| B. | 标准状况下,11g3H216O种含有的质子数为6NA | |
| C. | 1molLi2O和Na2O2的混合物中含有的离子总数为3NA | |
| D. | 1molN2与足量H2混合,充分反映后转移电子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
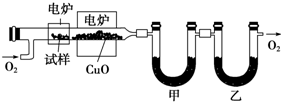
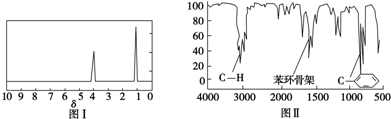
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
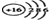 .
. ;B与D形成的化合物BD2的结构式是O=C=O,BD2属于共价(填“离子”或“共价”)化合物.
;B与D形成的化合物BD2的结构式是O=C=O,BD2属于共价(填“离子”或“共价”)化合物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
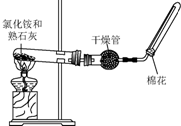 A、B、C、D是中学化学常见的四种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).
A、B、C、D是中学化学常见的四种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
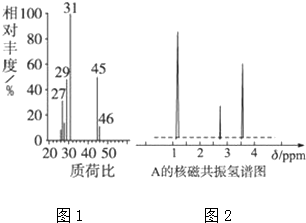
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com