
分析 (1)用焦炭作还原剂,在高温下用该矿石可制得粗锡,同时得到一氧化碳;
(2)马口铁是在铁皮表面镀一层金属锡,铁比锡活泼,形成原电池中铁做负极失电子发生氧化反应生成亚铁离子;
(3)①Sn2+易水解、易被氧化,所以实验室配制SnCl2溶液时要防止其水解及发生氧化反应;
②SnCl4水解得到Sn(OH)4与HCl,HCl与氨气反应得到NH4Cl;
(4)Sn(OH)2具有明显的两性,在碱性条件下以Sn(OH)3的形式存在,结合水中氢氧根生成氢离子;
(5)SnS2是黄色固体,俗称“金粉”,将H2S通入SnCl4溶液中可得SnS2沉淀,结合原子守恒和电荷守恒书写离子方程式;
(6)Fe2(SO4)3将Sn2+全部氧化为Sn4+,再用溶液K2Cr2O7溶液滴定,将Fe2+氧化为Fe3+,
解答 解:(1)用焦炭作还原剂,在高温下用该矿石可制得粗锡,根据反应物和生成物,利用质量守恒定律可写出化学方程式为:SnO2+2C$\frac{\underline{\;高温\;}}{\;}$Sn+2CO,
故答案为:SnO2+2C$\frac{\underline{\;高温\;}}{\;}$Sn+2CO;
(2)马口铁是在铁皮表面镀一层金属锡,铁比锡活泼,形成原电池中铁做负极失电子发生氧化反应生成亚铁离子,负极上的电极反应是:Fe-2e-=Fe2+,
故答案为:Fe-2e-=Fe2+;
(3)①Sn2+易水解、易被氧化,所以实验室配制SnCl2溶液时要防止其水解及发生氧化反应,要先将SnCl2固体溶于少量浓盐酸中,并在新配制的SnCl2溶液中加入少量锡粉,
故答案:将SnCl2固体溶于较浓的少量盐酸中,然后加适量水稀释,并加入少量锡粒;
②SnCl4水解得到Sn(OH)4与HCl,HCl与氨气反应得到NH4Cl,反应方程式为:SnCl4+4NH3+4H2O=Sn(OH)4+4NH4Cl,
故答案为:SnCl4+4NH3+4H2O=Sn(OH)4+4NH4Cl;
(4)Sn(OH)2具有明显的两性,在碱性条件下以Sn(OH)3的形式存在,结合水中氢氧根生成氢离子,电离方程式为:Sn(OH)2+H2O?H++Sn(OH)3,
故答案为:Sn(OH)2+H2O?H++Sn(OH)3;
(5)SnS2是黄色固体,俗称“金粉”,将H2S通入SnCl4溶液中可得SnS2沉淀,反应的离子方程式为:2H2S+Sn4+=SnS2↓+4H+,故答案为:2H2S+Sn4+=SnS2↓+4H+;
(6)Fe2(SO4)3将Sn2+全部氧化为Sn4+,再用溶液K2Cr2O7溶液滴定,将Fe2+氧化为Fe3+,用离子方程式表示K2Cr2O7溶液进行滴定实验的原理为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,
故答案为:将Sn2+全部氧化为Sn4+;Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;
点评 本题属于拼合型题目,涉及物质制备方案、原电池反应、氧化还原反应、离子方程式书写等,是对学生综合能力的考查,需要学生具备扎实的基础与良好的心理素质,题目难度中等.


 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径由大到小的顺序为R、Z、Y、W | |
| B. | X、Y分别与Z形成的多种化合物中化学键类型相同 | |
| C. | Y、R分别与X形成的化合物沸点依次升高 | |
| D. | Z、W、R最高价氧化物对应的水化物两两之间均能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜长期放置在潮湿的空气中容易生锈,生成Cu(OH)2 | |
| B. | 铜丝在氯气中燃烧生成CuCl2而与硫反应生成Cu2S,说明氧化性Cl2>S | |
| C. | CuO不及Cu2O稳定,高温条件下CuO可以分解生成Cu2O和氧气 | |
| D. | 蓝色的CuSO4•5H2O可以受热分解转化为白色的CuSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| R | 原子最外层电子数是电子总数的$\frac{2}{3}$ |
| X | 单质不能将比它不活泼的金属从其盐溶液中置换出来 |
| Y | 第三周期原子半径最小的金属 |
| Z | 单质是淡黄色固体 |
| A. | R的最高价氧化物既能与某种非金属单质反应,又能与某种金属单质反应 | |
| B. | X、Y、Z的氧化物分别投入NaOH溶液中一定都能发生反应 | |
| C. | X、Y、Z的原子半径依次减小,离子半径依次增大 | |
| D. | X、Y、Z的最高价氧化物对应水化物之间可以两两反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y只能形成一种化合物 | |
| B. | 最高价氧化物对应水化物的酸性:N>M | |
| C. | 单质与水反应的剧烈程度:Z>Y | |
| D. | X和M的最高正价相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 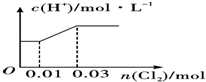 | B. |  | ||
| C. | 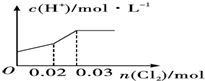 | D. | 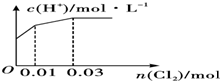 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
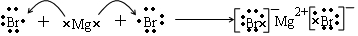 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com