
·ÖĪö £Ø1£©Õż·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶ČĘ½ŗāÄęĻņŅĘ¶Æ£¬Ę½ŗā³£Źż¼õŠ”£»
£Ø2£©¢Ł·“Ó¦»ģŗĻĪļø÷ĪļÖŹµÄĮæĻµŹżĻąĶ¬¶¼ĪŖ1£¬ĄūÓĆĪļÖŹµÄĮæ“śĢęÅØ¶Č¼ĘĖć“ĖŹ±ÅضČÉĢQc£¬ČōQc=K£¬“¦ÓŚĘ½ŗāדĢ¬£¬ČōQc£¼K£¬·“Ó¦ĻņÕż·“Ó¦½ųŠŠ£¬ČōQc£¾K£¬·“Ó¦ĻņÄę·“Ó¦½ųŠŠ£»
¢ŚÓĆx±ķŹ¾³öÅضČÉĢQc£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬ÅضČÉĢŠ”ÓŚĘ½ŗā³£Źż£»
£Ø3£©Ōö“óŅ»ÖÖÉś²śĪļ£ØĒāĘų£©µÄĢå»ż·ÖŹż£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬Ę½ŗāŅĘ¶ÆµÄ½į¹ūŹĒ½µµĶÕāÖÖŌö“óµÄ·ł¶Č£¬¹ŹĘ½ŗāŗóĒāĘųµÄĢå»ż·ÖŹż»¹ŹĒ“óÓŚŌĄ“µÄ£®
½ā“š ½ā£ŗ£Ø1£©Õż·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶ČĘ½ŗāÄęĻņŅĘ¶Æ£¬Ę½ŗā³£Źż¼õŠ”£¬ČōÉżøßĪĀ¶Čµ½950”ę£¬“ļµ½Ę½ŗāŹ±K£¼1£¬¹Ź“š°øĪŖ£ŗŠ”ÓŚ£»
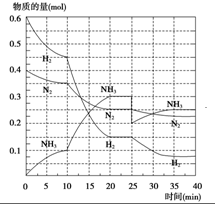
£Ø2£©¢ŁÓ¦»ģŗĻĪļø÷ĪļÖŹµÄĮæĻµŹżĻąĶ¬¶¼ĪŖ1£¬ĄūÓĆĪļÖŹµÄĮæ“śĢęÅØ¶Č¼ĘĖćÅضČÉĢ£¬“ĖŹ±µÄÅضČÉĢQc=$\frac{5”Į1}{1”Į3}$=1.67£¾K=1£¬·“Ó¦ĻņÄę·“Ó¦½ųŠŠ£¬¹Ź“š°øĪŖ£ŗÄę·“Ó¦£»
¢ŚĘ½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬ÅضČÉĢŠ”ÓŚĘ½ŗā³£Źż£¬¼“$\frac{1”Įx}{1”Į3}$£¼1£¬½āµĆx£¼3£¬¼“0”Üx£¼3£¬¹Ź“š°øĪŖ£ŗ0”Üx£¼3£»
£Ø3£©Ōö“óŅ»ÖÖÉś²śĪļ£ØĒāĘų£©µÄĢå»ż·ÖŹż£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬Ę½ŗāŅĘ¶ÆµÄ½į¹ūŹĒ½µµĶÕāÖÖŌö“óµÄ·ł¶Č£¬¹ŹĘ½ŗāŗóĒāĘųµÄĢå»ż·ÖŹż»¹ŹĒ“óÓŚŌĄ“µÄ£¬Ōņa%£¼b%£¬¹Ź“š°øĪŖ£ŗ£¼£»
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗā¼ĘĖć£¬Ę½ŗā³£Źż¼°ĘäÓ¦ÓĆµČ£¬×¢Ņā»ÆŃ§Ę½ŗā³£ŹżÖ»ÓėĪĀ¶ČÓŠ¹Ų£¬Óė·“Ó¦ĪļÅØ¶Č”¢ŹĒ·ńŹ¹ÓĆ“ß»Æ¼ĮĪŽ¹Ų£¬ĪĀ¶Č²»±ä£¬»ÆŃ§Ę½ŗā³£Źż²»±ä£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŌµŲ¹µÓĶĪŖŌĮĻ¼Ó¹¤ÖĘ³ÉµÄÉśĪļ²ńÓĶµÄ³É·ÖÓė“ÓŹÆÓĶ·ÖĮóµĆµ½µÄ²ńÓĶ³É·Ö²»Ķ¬ | |
| B£® | ŌŚŹ³Ę·“üÖŠ·ÅČėŹ¢ÓŠ¹č½ŗŗĶĢś·ŪµÄĶøĘųŠ”“ü£¬æÉ·ĄÖ¹Ź³ĪļŹÜ³±”¢Ńõ»Æ±äÖŹ | |
| C£® | ĀĢÉ«»ÆѧµÄŗĖŠÄŹĒÓ¦ÓĆ»ÆѧŌĄķ¶Ō»·¾³ĪŪČ¾½ųŠŠÖĪĄķ | |
| D£® | ĢģČ»Ęų”¢ÕÓĘųŗĶĖ®ĆŗĘų·Ö±šŹōÓŚ»ÆŹÆÄÜŌ“”¢æÉŌŁÉśÄÜŌ“ŗĶ¶ž“ĪÄÜŌ“ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Ģ¼Ėį±µæÉÓĆÓŚÖĪĮĘĪøĖį¹ż¶ąµÄŅ© | |
| B£® | ¶žŃõ»ÆĮņæÉÓĆ×÷Ź³Ę·µÄĘÆ°×¼Į | |
| C£® | Ģ¼ĻĖĪ¬ŹĒø“ŗĻ²ÄĮĻ | |
| D£® | PM2.5ÖøŹżŹĒĪķö²ĢģĘų¼ą²āÖŠµÄÖŲŅŖÖø±ź |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃéÄæµÄ | ŹµŃé¹ż³Ģ |
| A | Ö¤Ć÷¹¹³ÉŌµē³ŲÄܼÓæģÖĘČ”ĒāĘųĖŁĀŹ | ŌŚŠæÓėĻ”ĮņĖį·“Ó¦Ź±¼Ó×ćĮæŃõ»ÆĶ |
| B | Ö¤Ć÷øŗ¼«·¢ÉśŃõ»Æ·“Ó¦£¬Õż¼«·¢Éś»¹Ō·“Ó¦ | ½«Šæʬ”¢Ķʬ·Ö±š·ÅČėĮņĖįĶČÜŅŗÖŠ |
| C | Ö¤Ć÷µē¼«ĄąŠĶÓėµē½āÖŹČÜŅŗÓŠ¹Ų | ŅŌĀĮ”¢Ć¾ĪŖµē¼«£¬·Ö±šŌŚĒāŃõ»ÆÄĘČÜŅŗ”¢Ļ”ĮņĖįÖŠ¹¹³ÉŌµē³Ų |
| D | Ö¤Ć÷Ag+µÄŃõ»ÆŠŌ±ČCu2+Ēæ | ŅŌŹÆÄ«ĪŖµē¼«£¬µē½ā0.001mol•L-1AgNO3ČÜŅŗŗĶ1mol•L-Cu£ØNO3£©2ČÜŅŗ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 °±ŹĒÖŲŅŖµÄµŖ·Ź£¬ŗĻ³ÉŌĄķĪŖ£ŗN2£Øg£©+3H2£Øg£©øßĪĀ”¢øßŃ¹“߻ƼĮ
°±ŹĒÖŲŅŖµÄµŖ·Ź£¬ŗĻ³ÉŌĄķĪŖ£ŗN2£Øg£©+3H2£Øg£©øßĪĀ”¢øßŃ¹“߻ƼĮ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com