
 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-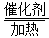 4NO+6H2O
4NO+6H2O Cl2↑+H2↑+2OH-
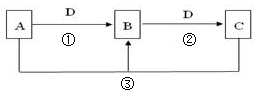
Cl2↑+H2↑+2OH- 4NO+6H2O。(3)若D是氯碱工业的主要产品,B有两性,由转化关系D为NaOH,B为Al(OH)3,C为NaAlO2,反应②的离子方程式是Al(OH)3+OH-=AlO2-+2H2O。
4NO+6H2O。(3)若D是氯碱工业的主要产品,B有两性,由转化关系D为NaOH,B为Al(OH)3,C为NaAlO2,反应②的离子方程式是Al(OH)3+OH-=AlO2-+2H2O。

科目:高中化学 来源:不详 题型:单选题
| A.石墨 | B.二氧化硅 | C.氧化镁 | D.氧化铝 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
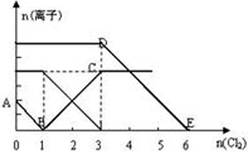
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
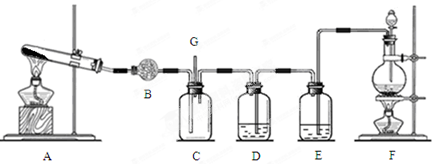
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.溴水中存在着如下的平衡:Br2+H2O HBr+HBrO,若要使溴水的颜色变浅,可采取的措施是加入NaI晶体 HBr+HBrO,若要使溴水的颜色变浅,可采取的措施是加入NaI晶体 |
| B.在温水瓶中加入Na2CO3溶液泡浸后加入盐酸能除去内壁CaSO4 |
| C.用饱和的NaOH热溶液除去乙酸乙酯中的乙醇、乙酸 |
| D.亚硫酸钠具有较强的还原性,检验亚硫酸钠试样是否变质: |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.K+、SiO32-、Cl-、NO3- |
| B.H+、NH4+、Al3+、SO42- |
| C.Na+、Cl-、MnO4-、SO42- |
| D.Na+、CO32-、CH3COO-、HCO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

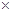 10-2mol·L-1,II中反应所得NaClO2溶液(含少量NaOH)的pH=13,则溶液中
10-2mol·L-1,II中反应所得NaClO2溶液(含少量NaOH)的pH=13,则溶液中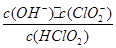 = 。
= 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com