
| ���� | �۵�/�� | �е�/�� | ��ѧ���� | ||||
| S | 112.8 | 444.6 | �� | ||||
| S2Cl2 | -77 | 137 | ��ˮ����HCl��SO2��S��300��������ȫ�ֽ⣻ S2Cl2+Cl2
|
| ||
| ||
| ||
| ||


 �㽭֮�ǿ�ʱ�Ż���ҵϵ�д�
�㽭֮�ǿ�ʱ�Ż���ҵϵ�д� ����˼ά�żӿ���ϵ�д�
����˼ά�żӿ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״���£�22.4 L NO��11.2 L O2��ַ�Ӧ��õ������������ΪNA |
| B��3.6 g��ˮ�к��е�������Ϊ2NA |
| C��һ�������£�6.4 gͭ���������Ӧ��ת�Ƶ�����ĿΪ0.2NA |
| D�������£�1 L 1 mol?L-1��CH3COOH��Һ�У��������ʷ�����С��NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
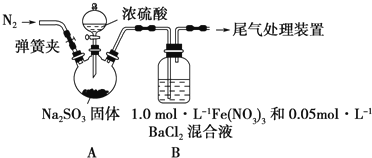
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
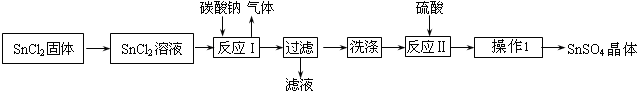
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �̼��仯����Ӧ��Խ��Խ�㷺��MnO2��һ����Ҫ�������ܲ��ϣ��Ʊ�Mn02�ķ���֮һ����ʯīΪ�缫������ữ��MnS04��Һ�������ĵ缫��ӦʽΪ
�̼��仯����Ӧ��Խ��Խ�㷺��MnO2��һ����Ҫ�������ܲ��ϣ��Ʊ�Mn02�ķ���֮һ����ʯīΪ�缫������ữ��MnS04��Һ�������ĵ缫��ӦʽΪ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ѡ������ʱ��ʹ��240 mL����ƿ |
| B�����ձ����ѻָ������µ�����������Һע��δ������Ľྻ����ƿ�� |
| C���������õ��������ƹ����������ƿ�У���������ˮ�ܽ� |
| D����ҡ�Ⱥ���Һ������˿̶��ߣ������ý�ͷ�ιܵμ����̶����밼Һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �о�CO2�����öԴٽ���̼���Ĺ���������Ҫ�����壮
�о�CO2�����öԴٽ���̼���Ĺ���������Ҫ�����壮�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com