
【题目】2008年9月27日16﹕43,中国人走出由中国人自主研制的航天飞船,进行包括科学实验在内的出舱活动。标志着中国已经成为世界上继俄、美之后第三个能够进行飞船舱外活动的国家。在飞船的火箭推进器中常装有液态肼(用A表示)和过氧化氢(H2O2),它们混合时的反应方程式为:2H2O2+A=N2+4H2O,则肼(A)的化学式为
A. N2H2 B. N2H4 C. NH2 D. N2H4O2
科目:高中化学 来源: 题型:
【题目】【化学——选修物质结构与性质】
X是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y基态原子的3p轨道上有2个未成对电子。元素Z 的原子最外层电子数是其内层的3倍。回答下列问题:
(1)元素X在元素周期表中位于 区,单质X的晶体类型为 ,其中X原子的配位数为 。
(2)已知元素Y可与元素Z的相对原子质量只差为16,则元素Y基态原子的外围电子排布图为 ,其同周期元素中,第一电离能最大的是________________(写元素符号)。元素Y的含氧酸中,酸性最强的是_____________(写化学式),该酸根离子的立体构型为_____________。
(3)Z的氢化物在乙醇中的溶解度大于Y的氢化物,其原因是 。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 。
(5)X与Y形成的一种化合物的立方晶胞如图所示。
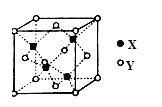
该化合物的化学式为_______________,已知此晶体的密度为ρg·cm–3,阿伏伽德罗常数为NA,则此晶胞中X与Y的最近距离是 cm。(写出计算式,不要求计算结果。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某pH=1的ZnCl2和HCl的混合溶液中含有FeCl3杂质,通过水解除去杂质,需将溶液调至pH=4,在调节溶液pH时,应选用的试剂是
A.NaOHB.ZnOC.Na2CO3D.Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环己醇(![]() )常用来制取增塑剂和作为工业溶剂。下列说法正确的是( )
)常用来制取增塑剂和作为工业溶剂。下列说法正确的是( )
A. 环己醇中至少有12个原子共平面
B. 与环己醇互为同分异构体,且含有醛基(—CHO)的结构有8种(不含立体结构)
C. 标准状况下,1mol环己醇与足量Na反应生成22.4LH2
D. 环己醇的一氯代物有3种(不含立体结构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
铍及其化合物的应用正日益被重视。
(l)最重要的含铍矿物是绿柱石,含2%铬(Cr)的绿柱石即为祖母绿。基态Cr原子价电子的轨道表示式为__________。
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有_____(填标号)。
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液pH均小于7
(3)铍、铝晶体都是由金属原子密置层在三维空间堆积而成(最密堆积)。铍的熔点(155lK)比铝的熔点(930K)高,原因是______________。
(4)氯化铍在气态时存在BeC12分子(a)和二聚分子(BeCl2)2(b),固态时则具有如下图所示的链状结构(c)。
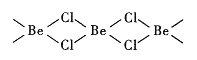
① a属于__________(填“极性”或“非极性”)分子。
② b中Be原子的杂化方式相同,且所有原子都在同一平面上。b 的结构式为____ (标出配位键)。
③ c中Be原子的杂化方式为__________。
④ 氯化铍晶体中存在的作用力有__________(填标号)。
A.范德华力 B. σ键 C.极性键 D.非极性键 E.离子键
(5)BeO立方晶胞如下图所示。
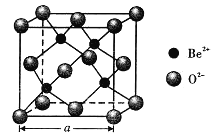
① BeO晶体中,O2-的配位数为___________。
② 若BeO晶体的密度为dg/cm3,则晶胞参数a =______nm (列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学键的各种叙述中正确的是( )
A.在离子化合物里,只存在离子键 B.非极性键只存在于双原子的单质分子里
C.共价化合物里,一定不存在离子键 D.不同元素组成的多原子分子里,只存在极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填写下列空白[第(1)~(4)小题用元素符号填写]。
(1)第三周期原子半径最小的元素________。
(2)第一电离能最大的元素________。
(3)电负性最大的元素________。
(4)第四周期中第一电离能最小的元素________。
(5)含有8个质子,10个中子的原子的化学符号________。
(6)最外层电子排布为4s24p1的原子的核电荷数为________。
(7)周期表中最活泼的非金属元素原子的轨道表示式为___________________。
(8)某元素核外有三个电子层,最外层电子数是核外电子总数的![]() ,写出该元素原子的电子排布式是__________________。
,写出该元素原子的电子排布式是__________________。
(9)写出铜元素在周期表中的位置________________,它位于________区。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如图所示,图中含酚废水中有机物可用C6H5OH 表示,左、中、右室间分别以离子交换膜分隔。下列说法不正确的是( )
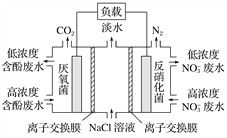
A. 右室电极为该电池的正极
B. 左室电极反应式可表示为C6H5OH-28e-+11H2O===6CO2↑+28H+
C. 右室电极附近溶液的pH减小
D. 工作时中间室的Cl-移向左室,Na+移向右室
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F对花香和果香具有提升作用,故常用于化妆品工业和食品工业。有机物F可以用下面的设计方案合成。
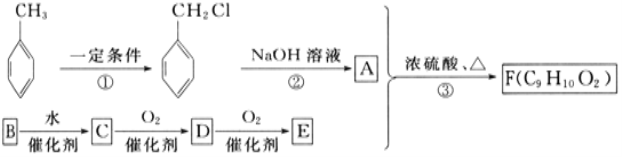
请回答下列问题:
(1)写出A的结构简式:_________________。
(2)①的反应类型:_______________。
(3)写出反应③的化学方程式:_________________________________________。
(4)F的同分异构体中含有—COO—的一取代苯结构有多个。请写出其中能发生银镜反应的两种物质的结构简式______________、___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com