
| 1000ρω |
| M |
| V |
| Vm |
| bc |
| a |
| bc |
| a?NA |
| bc |
| aNA |
| 22.4bc |
| a?NA |
| 22.4bc |
| a?NA |
| 1000×1.84×98% |
| 98 |
| 0.2mol |
| 0.1L |
| 3 |
| 2 |
| 1000mL×1.18g/cm3×5.6% |
| 24g/mol |


科目:高中化学 来源: 题型:
| A、当△H为负值时,表示该反应为吸热反应 |
| B、燃烧不一定是放热反应 |
| C、反应热的大小与反应物所具有的能量和生成物具有的能量无关 |
| D、反应热的大小只与反应体系的始态和终态有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | A | B | C | D |
| 分类 | 单质 | 盐 | 胶体 | 强电解质 |
| 物质 | 液溴、碘(I2)、钢 | 食盐、生石灰、小苏打 | 牛奶、淀粉溶液、氢氧化铁胶体 | 醋酸、纯碱、烧碱 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 mol、64 mol、24 mol |
| B、64 mol、2 mol、24 mol |
| C、32 mol、50 mol、12 mol |
| D、16 mol、50 mol、24 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 操作 | 现象 | 结论 |
| A | 在AlCl3溶液中滴加过量氨水 | 有白色沉淀生成 | 实验室常用此法制备Al(OH)3 |
| B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
| C | 将一小块Na放入CuSO4溶液中 | Na很快消失 | Na 能置换出铜盐溶液中的铜 |
| D | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A是一种重要的化工原料,它的一种合成路线如图所示:
A是一种重要的化工原料,它的一种合成路线如图所示:
| A、1mol双酚A最多可与2mol Br2反应 |
| B、G物质是乙醛的同系物 |
| C、E物质的名称是1-溴丙烷 |
D、反应③的化学方程式是 |
查看答案和解析>>
科目:高中化学 来源: 题型:
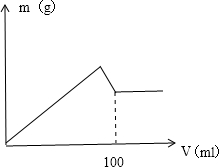 有AlCl3和MgCl2的固体混合物,取一定量的该混合物加水溶解配成溶液,实验测知Cl-的物质的量为0.70摩尔,如向该混合溶液中逐滴加入8.00mol/L的氢氧化钠溶液(密度为1.27g/ml),加入氢氧化钠溶液的体积(V)和沉淀的质量(m)有如图所示的关系.
有AlCl3和MgCl2的固体混合物,取一定量的该混合物加水溶解配成溶液,实验测知Cl-的物质的量为0.70摩尔,如向该混合溶液中逐滴加入8.00mol/L的氢氧化钠溶液(密度为1.27g/ml),加入氢氧化钠溶液的体积(V)和沉淀的质量(m)有如图所示的关系.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com