
”¾ĢāÄæ”æ¼×ĶéÓėŃõĘų·“Ó¦¹ż³ĢÖŠµÄÄÜĮæ±ä»ÆČēĻĀĶ¼ĖłŹ¾”£ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠÕżČ·µÄŹĒ
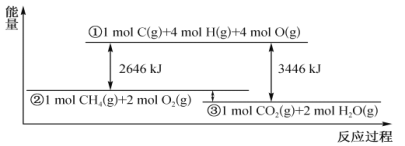
A. ·“Ó¦ CO2(g)+2H2O(l)==CH4(g)+2O2(g) ”÷H<0
B. Čō½«1mol CO2(g)”¢2 molH2O(l)µÄÄÜĮæ±źŌŚĶ¼ÖŠ£¬ŌņĘäĪ»ÖĆŌŚ¢Ł”¢¢ŚÖ®¼ä
C. ČōCŅ»H¼üµÄ¼üÄÜĪŖ415kJ mol-1£¬ŌņO= OµÄ¼üÄÜĪŖ493 kJ mol-1
D. ČōøĆ·“Ó¦¹ż³ĢÖŠ×Ŗ»ÆµÄ»ÆѧÄÜĪŖ200kJ£¬ŌņÓŠ0.25 molC=OÉś³É
”¾“š°ø”æC
”¾½āĪö”æ
A.¼×ĶéµÄČ¼ÉÕ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬Ņņ“ĖCO2(g)+2H2O(l)==CH4(g)+2O2(g) ”÷H£¾0£¬¹ŹA“ķĪó£»
B.ŅŗĢ¬Ė®Ėłŗ¬µÄ×ÜÄÜĮæµĶÓŚĘųĢ¬Ė®Ėłŗ¬µÄ×ÜÄÜĮ棬¹ŹŌŚ¢ŪµÄĻĀ·½£¬¹ŹB“ķĪó£»
C.ÓÉĶ¼ĻóæÉÖŖĘĘ»µ4mol C-H¼üŗĶ2molO-O¼ü£¬ŠčŅŖĪüŹÕ2646kJÄÜĮ棬ĘäÖŠĘĘ»µ4mol C-H¼üŠčŅŖĪüŹÕ4”Į415kJ=1660kJÄÜĮ棬ĖłŅŌĘĘ»µ1molŃõĘųÖŠµÄ O=OÖŠµÄ»Æѧ¼üŠčŅŖĪüŹÕµÄÄÜĮæĪŖ![]() (2646-1660)kJ=493kJ£¬¹ŹCÕżČ·£»
(2646-1660)kJ=493kJ£¬¹ŹCÕżČ·£»
D.×ÜÄÜĮæÖ®²ī=Éś³ÉĪļ×ÜÄÜĮæ-·“Ó¦Īļ×ÜÄÜĮ棬¹Ź1mol CH4 (g)ŗĶ2mol O2(g)µÄ×ÜÄÜĮæÖ®²īĪŖ(3446-2646)=800kJ£»1molCH4 ²ĪÓė·“Ó¦·Å³ö800kJµÄČČĮ棬µ±ÄÜĮæ±ä»ÆĪŖ200kJŹ±£¬Ōņ²ĪÓė·“Ó¦µÄCH4 0.25mol£¬¾ŻŌŖĖŲŹŲŗć£¬ŌņÉś³É0.25molCO2£¬CO2½į¹¹¼ņŹ½ĪŖO=C=O£¬¹ŹÓŠ0.5molO=C¼üÉś³É£¬¹ŹD“ķĪó£»
“š°øŃ”C”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĆĄ¹śLawrece Liermore¹ś¼ŅŹµŃéŹŅ£ØLINL£©³É¹¦µŲŌŚøßŃ¹ĻĀ½«![]() ×Ŗ»ÆĪŖ¾ßÓŠĄąĖĘ
×Ŗ»ÆĪŖ¾ßÓŠĄąĖĘ![]() ½į¹¹µÄŌ×Ó¾§Ģ壬ĻĀĮŠ¹ŲÓŚ
½į¹¹µÄŌ×Ó¾§Ģ壬ĻĀĮŠ¹ŲÓŚ![]() µÄŌ×Ó¾§ĢåĖµ·Ø£¬ÕżČ·µÄŹĒ£ŗ
µÄŌ×Ó¾§ĢåĖµ·Ø£¬ÕżČ·µÄŹĒ£ŗ
A. ![]() µÄŌ×Ó¾§ĢåŗĶ·Ö×Ó¾§Ģ廄ĪŖĶ¬·ÖŅģ¹¹Ģå
µÄŌ×Ó¾§ĢåŗĶ·Ö×Ó¾§Ģ廄ĪŖĶ¬·ÖŅģ¹¹Ģå
B. ŌŚŅ»¶ØĢõ¼žĻĀ£¬![]() Ō×Ó¾§Ģå×Ŗ»ÆĪŖ
Ō×Ó¾§Ģå×Ŗ»ÆĪŖ![]() ·Ö×Ó¾§ĢåŹĒĪļĄķ±ä»Æ
·Ö×Ó¾§ĢåŹĒĪļĄķ±ä»Æ
C. ![]() µÄŌ×Ó¾§ĢåŗĶ
µÄŌ×Ó¾§ĢåŗĶ![]() ·Ö×Ó¾§Ģå¾ßÓŠĻąĶ¬µÄĪļĄķŠŌÖŹŗĶ»ÆѧŠŌÖŹ
·Ö×Ó¾§Ģå¾ßÓŠĻąĶ¬µÄĪļĄķŠŌÖŹŗĶ»ÆѧŠŌÖŹ
D. ŌŚ![]() µÄŌ×Ó¾§ĢåÖŠ£¬ĆæŅ»øöCŌ×ÓÖÜĪ§½įŗĻ4øöOŌ×Ó£¬ĆæŅ»øöOŌ×ÓøśĮ½øöCŌ×ÓĻą½įŗĻ
µÄŌ×Ó¾§ĢåÖŠ£¬ĆæŅ»øöCŌ×ÓÖÜĪ§½įŗĻ4øöOŌ×Ó£¬ĆæŅ»øöOŌ×ÓøśĮ½øöCŌ×ÓĻą½įŗĻ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧæĪĶāŠĖȤŠ”×éĪŖĢ½¾æĶøśÅØĮņĖįµÄ·“Ó¦Ēéæö£¬ÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠÓŠ¹ŲŹµŃé£ŗ

(1)BŹĒÓĆĄ“ŹÕ¼ÆŹµŃéÖŠ²śÉśµÄĘųĢåµÄ×°ÖĆ£¬µ«Ī“½«µ¼¹Ü»Č«£¬ĒėŌŚĶ¼ÉĻ°Ńµ¼¹Ü²¹³äĶźÕū_________”£
(2)ŹµŃéÖŠĖūĆĒČ”6.4 gĶʬŗĶ12 mL 18 mol”¤L1ÅØĮņĖį·ÅŌŚŌ²µ×ÉÕĘæÖŠ¹²ČČ£¬Ö±µ½·“Ó¦Ķź±Ļ£¬×īŗó·¢ĻÖÉÕĘæÖŠ»¹ÓŠĶʬŹ£Óą£¬øĆŠ”×éѧɜøł¾ŻĖłŃ§µÄ»ÆѧÖŖŹ¶ČĻĪŖ»¹ÓŠŅ»¶ØĮæµÄĮņĖįŹ£Óą”£
¢ŁŠ“³öĶøśÅØĮņĖį·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ__________________£»
¢ŚĪŖŹ²Ć“ÓŠŅ»¶ØĮæµÄÓąĖįµ«Ī“ÄÜŹ¹ĶʬĶźČ«Čܽā£¬ÄćČĻĪŖŌŅņŹĒ__________________£»
¢ŪĻĀĮŠŅ©Ę·ÖŠÄܹ»ÓĆĄ“Ö¤Ć÷·“Ó¦½įŹųŗóµÄÉÕĘæÖŠČ·ÓŠÓąĖįµÄŹĒ________(Ģī±ąŗÅ)”£
A£®Ģś·Ū B£®BaCl2ČÜŅŗ C£®Ņų·Ū D£®Na2CO3ČÜŅŗ
(3)×°ÖĆCÖŠŹŌ¹ÜDÄŚŹ¢×°µÄŹĒĘ·ŗģČÜŅŗ£¬µ±BÖŠĘųĢåŹÕ¼ÆĀśŗó£¬ÓŠæÉÄܹŪ²ģµ½µÄĻÖĻóŹĒ_____________£¬“ż·“Ó¦½įŹųŗó£¬ĻņCÖŠÉÕ±ÄŚ¼ÓČė·ŠĖ®£¬DÖŠ¹Ū²ģµ½µÄĻÖĻóŹĒ_____________”£
(4)ŹµŃé×°ÖĆCÓŠæÉÄÜŌģ³É»·¾³ĪŪČ¾£¬ŹŌÓĆ×ī¼ņµ„µÄ·½·Ø¼ÓŅŌ½ā¾ö£¬__________________(ŹµŃéÓĆĘ·×ŌŃ”)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓū²ā¶Ø½šŹōĆ¾µÄĻą¶ŌŌ×ÓÖŹĮ棬ĒėĄūÓĆĻĀĶ¼øų¶ØµÄŅĒĘ÷×é³ÉŅ»Ģ׏µŃé×°ÖĆ(ĆæøöŅĒĘ÷Ö»ÄÜŹ¹ÓĆŅ»“Ī£¬¼ŁÉčĘųĢåµÄĢå»żæÉæ“×÷±ź×¼×“æöĻĀµÄĢå»ż)”£

ĢīŠ“ĻĀĮŠø÷Ļī(ĘųĮ÷“Ó×óµ½ÓŅ)£ŗ
(1)ø÷ÖÖŅĒĘ÷Į¬½ÓµÄĻČŗóĖ³ŠņŹĒ__________½Ó________”¢________½Ó________”¢________½Ó________”¢________½Ó________(ÓĆŠ”Š“×ÖÄø±ķŹ¾)”£
(2)Į¬½ÓŗĆŅĒĘ÷ŗó£¬ŅŖ½ųŠŠµÄ²Ł×÷ÓŠŅŌĻĀ¼ø²½£¬ĘäĻČŗóĖ³ŠņŹĒ________________(ĢīŠņŗÅ)”£
¢Ł“żŅĒĘ÷BÖŠµÄĪĀ¶Č»Öø“ÖĮŹŅĪĀŹ±£¬²āµĆĮæĶ²CÖŠĖ®µÄĢå»żĪŖVa mL£»
¢Ś²ĮµōĆ¾Ģõ±ķĆęµÄŃõ»ÆĤ£¬½«ĘäÖĆÓŚĢģĘ½ÉĻ³ĘĮ棬µĆÖŹĮæĪŖm g£¬²¢½«ĘäĶ¶ČėŹŌ¹ÜBÖŠµÄ“ųæ×øō°åÉĻ£»
¢Ū¼ģ²é×°ÖƵÄĘųĆÜŠŌ£»
¢ÜŠżæŖ×°ÖĆAÉĻ·ÖŅŗĀ©¶·µÄ»īČū£¬Ź¹ĘäĖ®Ė³ĄūĮ÷ĻĀ£¬µ±Ć¾ĶźČ«ČܽāŹ±ŌŁ¹Ų±ÕÕāøö»īČū£¬ÕāŹ±AÖŠ¹²·ÅČėĖ®Vb mL”£
(3)øł¾ŻŹµŃ鏿¾ŻæÉĖć³ö½šŹōĆ¾µÄĻą¶ŌŌ×ÓÖŹĮ棬Ę䏿ѧ±ķ“ļŹ½ĪŖ___________________”£
(4)ČōŹŌ¹ÜBµÄĪĀ¶ČĪ“ĄäČ“ÖĮŹŅĪĀ£¬¾Ķ¶Į³öĮæĶ²CÖŠĖ®µÄĢå»ż£¬Õā½«»įŹ¹Ėł²ā¶ØĆ¾µÄĻą¶ŌŌ×ÓÖŹĮæŹż¾Ż________(Ģī”°Ę«“ó”±”°Ę«Š””±»ņ”°ĪŽÓ°Ļģ”±)”£
(5)׊Ļø·ÖĪöÉĻŹöŹµŃé×°ÖĆŗ󣬾ĢÖĀŪČĻĪŖ½į¹ū»įÓŠĪó²ī£¬ÓŚŹĒÓÖÉč¼ĘĮĖČēĻĀĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆ”£

¢Ł×°ÖĆÖŠµ¼¹ÜaµÄ×÷ÓĆŹĒ_________________________________________”£
¢ŚŹµŃéĒ°ŗó¼īŹ½µĪ¶Ø¹ÜÖŠŅŗĆę¶ĮŹż·Ö±šĪŖV1 mL”¢V2 mL”£Ōņ²śÉśĒāĘųµÄĢå»żĪŖ____________mL”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³Ń§ÉśĄūÓĆŅŌĻĀ×°ÖĆĢ½¾æĀČĘųÓė°±ĘųÖ®¼äµÄ·“Ó¦”£ĘäÖŠCĪŖ“æ¾»øÉŌļµÄĀČĘųÓė°±Ęų·“Ó¦µÄ×°ÖĆ”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
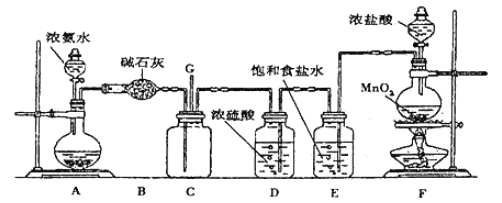
£Ø1£©×°ÖĆAÖŠµÄÉÕĘæÄŚ¹ĢĢå²»ÄÜŃ”ÓĆ_____________”£
A£®ÉśŹÆ»Ņ B£®¼īŹÆ»Ņ
C£®ĪåŃõ»Æ¶žĮ× D£®ÉÕ¼ī
£Ø2£©×°ÖĆAÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ________________________”£
£Ø3£©B×°ÖƵÄ×÷ÓĆ_____________£»E×°ÖƵÄ×÷ÓĆ_____________”£
£Ø4£©×°ÖĆCÄŚ³öĻÖÅØŗńµÄ°×ŃĢ²¢ŌŚČŻĘ÷ÄŚ±ŚÄż½į£¬ĮķŅ»Éś³ÉĪļŹĒæÕĘųµÄÖ÷ŅŖ³É·ÖÖ®Ņ»”£Š“³ö·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ___________”£
£Ø5£©“Ó×°ÖĆCµÄG“¦ŅŻ³öµÄĪ²ĘųÖŠæÉÄÜŗ¬ÓŠ»ĘĀĢÉ«µÄÓŠ¶¾ĘųĢ壬ŠčŅŖ“¦Ąķ£¬Š“³öĄė×Ó·½³ĢŹ½________________£»
ŹµŃéŹŅÖʱø°±Ęų£¬ĻĀĮŠ·½·ØÖŠŹŹŅĖŃ”ÓƵďĒ________________________”£
¢Ł¹ĢĢ¬ĀČ»Æļ§¼ÓČČ·Ö½ā
¢ŚÅØ°±Ė®ÖŠ¼ÓČė¹ĢĢåĒāŃõ»ÆÄĘ
¢Ū¼ÓČČÅØ°±Ė®
¢Ü¹ĢĢ¬ĀČ»Æļ§ÓėĒāŃõ»ÆøĘ»ģŗĻ¼ÓČČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŅĻ©ŹĒÖŲŅŖµÄÓŠ»ś»Æ¹¤ŌĮĻ£¬æÉÓÉŅŅ“¼ĶŃĖ®Öʱø”£Éę¼°·“Ó¦ČēĻĀ£ŗ
¢Ł2CH3OH(g)![]() CH3OCH3(g)+ H2O(g) ”÷H1=”Ŗ23.9 kJmol-1
CH3OCH3(g)+ H2O(g) ”÷H1=”Ŗ23.9 kJmol-1
¢Ś2CH3OH(g)![]() C2H4(g)+2H2O(g) ”÷H2= ”Ŗ29.1kJmol-1
C2H4(g)+2H2O(g) ”÷H2= ”Ŗ29.1kJmol-1
¢ŪCH3CH2OH(g)![]() CH3OCH3(g) ”÷H3= +50.7kJmol-1
CH3OCH3(g) ”÷H3= +50.7kJmol-1
¢ÜC2H5OH(g)![]() C2H4(g)+ H2O(g) ”÷H4=akJmol-1
C2H4(g)+ H2O(g) ”÷H4=akJmol-1
»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)a=___________ӣ
(2)ŌŚ1.0LĆܱÕČŻĘ÷ÖŠ·ÅČė0.10 mol C2H5OH(g)£¬ŌŚŅ»¶ØĪĀ¶ČĻĀ½ųŠŠ¢Ü·“Ó¦£¬·“Ó¦Ź±¼ä(t)ÓėČŻĘ÷ÄŚĘųĢå×ÜŃ¹Ēæ(P)µÄŹż¾Ż¼ūĻĀ±ķ£ŗ
Ź±¼ät/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
×ÜŃ¹ĒæP/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
¢ŁÓūĢįøßC2H5OHµÄĘ½ŗā×Ŗ»ÆĀŹ£¬Ó¦²ÉČ”µÄ“ėŹ©ĪŖ___________(Ģī×ÖÄø)”£
a.ÉżøßĪĀ¶Č b.Ōö“óŃ¹Ēæ
c.ĶØČėŅŅ“¼ d.½µµĶŃ¹Ēæ
¢ŚÓÉ×ÜŃ¹ĒæPŗĶĘšŹ¼Ń¹ĒæP0¼ĘĖć·“Ó¦ĪļC2H5OHµÄ×Ŗ»ÆĀŹ(C2H5OH)µÄ±ķ“ļŹ½ĪŖ_________£¬Ę½ŗāŹ±C2H5OHµÄ×Ŗ»ÆĀŹĪŖ_______(½į¹ū±£ĮōĮ½Ī»ÓŠŠ§Źż×Ö£¬ĻĀĶ¬)£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżK=_________”£
¢ŪÓĆ×ÜŃ¹ĒæPŗĶĘšŹ¼Ń¹ĒæP0±ķŹ¾·“Ó¦ĢåĻµµÄ×ÜĪļÖŹµÄĮæn(×Ü)ŗĶ·“Ó¦ĪļC2H5OHµÄĪļ ÖŹµÄĮæn(C2H5OH)£¬n(×Ü)=_____mol£¬n(C2H5OH)=_____mol”£
(3)ĻĀ±ķĪŖ·“Ó¦¢ÜÖŠ·“Ó¦ĪļÅضČÓė·“Ó¦Ź±¼äµÄŹż¾Ż£¬·ÖĪöøĆ·“Ó¦ÖŠc(C2H5OH)±ä»ÆÓėŹ±¼ä¼äøō(”÷t)µÄ¹ęĀÉ£¬µĆ³öµÄ½įĀŪŹĒ______£¬ÓÉ“Ė¹ęĀÉĶĘ³ö·“Ó¦ŌŚ12hŹ±c(C2H5OH)µČÓŚ______molL-1
·“Ó¦Ź±¼ät/h | 0 | 4 | 8 | 16 |
c(C2H5OH)/(molL-1) | 0.10 | 0.051 | 0.026 | 0.0065 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ŌÓŚ·“Ó¦£ŗ2SO2£«O2![]() 2SO3(g)£¬µ±ĘäĖūĢõ¼ž²»±äŹ±£¬Ö»øıäŅ»øö·“Ó¦Ģõ¼ž£¬½«Éś³ÉSO3µÄ·“Ó¦ĖŁĀŹµÄ±ä»ÆĢīČėĻĀ±ķæÕøńÄŚ(Ģī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±)”£
2SO3(g)£¬µ±ĘäĖūĢõ¼ž²»±äŹ±£¬Ö»øıäŅ»øö·“Ó¦Ģõ¼ž£¬½«Éś³ÉSO3µÄ·“Ó¦ĖŁĀŹµÄ±ä»ÆĢīČėĻĀ±ķæÕøńÄŚ(Ģī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±)”£
±ąŗÅ | øıäµÄĢõ¼ž | Éś³ÉSO3ĖŁĀŹ |
¢Ł | ÉżøßĪĀ¶Č | ________ |
¢Ś | ½µµĶĪĀ¶Č | ________ |
¢Ū | Ōö“óŃõĘųÅØ¶Č | ________ |
¢Ü | Ź¹ÓĆ“ß»Æ¼Į | ________ |
¢Ż | Ń¹ĖõĢå»ż | ________ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄĘĮņµē³ŲĢå»żŠ””¢ČŻĮæ“ó”¢ŹŁĆü³¤”¢Š§ĀŹøߣ¬ŌŚµēĮ¦“¢ÄÜÖŠ¹ć·ŗÓ¦ÓĆÓŚĻ÷·åĢī¹Č”¢Ó¦¼±µēŌ“”¢·ēĮ¦·¢µēµČ“¢ÄÜ·½Ćę”£Na-Sµē³ŲµÄ½į¹¹ČēĻĀĶ¼ĖłŹ¾£¬µē³Ų·“Ó¦ĪŖ2Na+![]() S8=Na2Sn”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
S8=Na2Sn”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
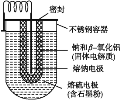
A. ČŪÄʵē¼«×÷µē³ŲµÄøŗ¼«B. ·ÅµēŹ±Na+ĻņÕż¼«ŅʶÆ
C. ³äµēŹ±ČŪÄʵē¼«ÓėµēŌ“µÄÕż¼«ĻąĮ¬D. ³äµēŹ±Ńō¼«·“Ó¦Ź½ĪŖ8Sn2--16e-=nS8
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ2015Äź10ŌĀ£¬ÖŠ¹śæĘѧ¼ŅĶĄßĻßĻŅņĪŖ““ÖĘĮĖŠĀŠĶæ¹Å±Ņ©©©ĒąŻļĖŲ£¬»ńµĆŵ±“¶ūÉśĄķѧ»ņŅ½Ń§½±£®ĒąŻļĖŲæÉÓÉĻćĆ©Č©ĪŖŌĮĻÖĘČ”£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
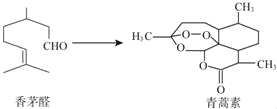
A£®ĻćĆ©Č©ÄÜŹ¹Br2µÄCCl4ČÜŅŗĶŹÉ«
B£®ĒąŻļĖŲ·Ö×ÓŹ½ĪŖC15H22O5
C£®ĒąŻļĖŲŌŚŅ»¶ØĢõ¼žĻĀæÉ·¢ÉśĖ®½ā·“Ó¦
D£®¶žÕß¾łæÉÓėĒāĘų·¢Éś¼Ó³É·“Ó¦
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com