
【题目】已知有机物CH3-CO-O-CH2-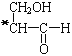 具有光学活性,若将该物质与某物质在一定条件下发生反应,使所得的生成物没有化学活性。根据你设计的反应写出无光学活性生成物的结构简式:__________________、__________________、__________________、__________________。
具有光学活性,若将该物质与某物质在一定条件下发生反应,使所得的生成物没有化学活性。根据你设计的反应写出无光学活性生成物的结构简式:__________________、__________________、__________________、__________________。
【答案】CH3-COO-CH2-CH(CHO)2CH3-COO-CH2-CH(CH2OH)2![]()
![]()
【解析】
使具有光学活性的物质转化为没有光学活性的物质,需要将其中的手性碳原子转变为非手性碳原子,主要是将手性碳原子上连接的四个不同的原子或原子团转化为相同的原子或原子团,据此分析可得结论。
将有机物CH3-CO-O-CH2-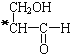 分子中的羟基催化氧化为醛基可得化合物:CH3-COO-CH2-CH(CHO)2,该物质中不再有手性碳原子;可将有机物中的醛基还原为羟基可得化合物:CH3-COO-CH2-CH(CH2OH)2,该物质中不再有手性碳原子;可将有机物与乙酸发生酯化反应得到化合物:
分子中的羟基催化氧化为醛基可得化合物:CH3-COO-CH2-CH(CHO)2,该物质中不再有手性碳原子;可将有机物中的醛基还原为羟基可得化合物:CH3-COO-CH2-CH(CH2OH)2,该物质中不再有手性碳原子;可将有机物与乙酸发生酯化反应得到化合物:![]() ,该物质中没有手性碳原子;可将有机物在酸性条件下水解得到有机物:
,该物质中没有手性碳原子;可将有机物在酸性条件下水解得到有机物:![]() ,该物质中不再有手性碳原子;故答案为:CH3-COO-CH2-CH(CHO)2、CH3-COO-CH2-CH(CH2OH)2、
,该物质中不再有手性碳原子;故答案为:CH3-COO-CH2-CH(CHO)2、CH3-COO-CH2-CH(CH2OH)2、![]() 、
、![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某有机物A的结构为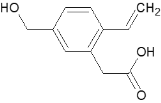 , 下列有关说法正确的是
, 下列有关说法正确的是
A. 1 mol A能跟2 mol NaOH溶液反应
B. 能发生加聚反应
C. 不能发生分子内酯化反应
D. A分子中所有原子在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关比较正确的是
A. N、O、F最高价依次升高 B. Al3+、K+、F- 微粒半径依次增大
C. 单质的熔点:Cl2>Br2>I2 D. 碱性:CsOH>KOH>NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物的说法不正确的是
A. 糖类物质均能发生水解反应
B. 酒精中是否含有水,不能用金属钠检验
C. 蛋白质在一定条件下能发生水解反应,生成氨基酸
D. 不能用米汤直接检验加碘食盐中是否含有碘元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)常用作氯化剂和氯磺化剂,在染料、药品、除草剂和农用杀虫剂的生产过程中有重要作用。现在拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =97.3 kJ·mol1,实验装置如图所示(部分夹持装置未画出)。

已知:硫酰氯通常条件下为无色液体,熔点54.1℃,沸点69.1℃。在潮湿空气中“发烟”;长期放置或者100°C以上发生分解,生成二氧化硫和氯气。回答下列问题:
(1)仪器C的名称是_______________,冷凝管的进水方向______(填“a”或“b”)。
(2)下列操作或描述正确的是_________________。
A.将70%硫酸换成98.3%硫酸,可以加快制取SO2的速率
B.实验中通过观察乙、丁导管口产生气泡的速率相等,可控制两种反应物体积相等
C.装置戊上方分液漏斗中最好选用0.10 molL-1NaCl溶液,减小氯气的溶解度
D.装置己防止污染,又防止硫酰氯变质
(3)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯,写出反应方程式:____________________。
(4)硫酰氯在潮湿空气中“发烟”,原因是_______________________(用化学方程式表示)。
(5)若反应中消耗的二氧化硫体积为560 mL(标准状况下),最后经过分离提纯得到2.7 g纯净的硫酰氯,则硫酰氯的产率为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示实验能达到实验目的的是

A. 利用甲装置制备少量O2 B. 利用乙装置制备无水氯化镁
C. 利用丙装置比较元素非金属性强弱 D. 利用丁装置收集氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧乙酸是人们常用的一种灭菌消毒剂。
(1)已知过氧化氢的结构式为H—O—O—H,其中的“一O—O—”称为过氧基,过氧乙酸可视为由过氧基取代乙酸分子中羟基上的氧原子而得到的产物。试写出过氧乙酸的结构式___________;
(2)过氧乙酸不稳定,在受热、光照等条件下,可发生分解,放出氧气,易引发火灾或爆炸事故,为防止分解,过氧乙酸应放置在___________处贮藏;
(3)过氧乙酸是一种强氧化剂,它可与乙烯反应生成环氧乙烷(![]() )和乙酸,环氧乙烷经水解可得一种重要的化工原料乙二醇,试分别写出上述两步反应的化学方程式:
)和乙酸,环氧乙烷经水解可得一种重要的化工原料乙二醇,试分别写出上述两步反应的化学方程式:
①_____________________________________________________________________;
②_____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铬铁矿(FeO、Cr2O3、含SiO2、Al2O3杂质)生产红矾钠(Na2Cr2O7)的工艺流程如下:
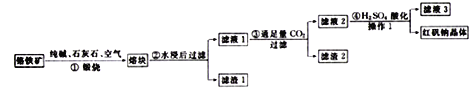
(1)上述四个步骤中,有氧化还原反应发生的是________(填序号),被氧化的元素是______(写元素符号)。
(2)滤渣1的主要成分是________(写化学式),写出步骤③发生反应的离子方程式___________________。
(3)操作1包括______、________、过滤、洗涤、干燥。
(4)向橙红色的红钒钠溶液中滴入氨氧化钠溶液,变为黄色Na2CrO4溶液,写出该转化过程的离子方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) 指出下列元素在周期表中的位置:硅在第_____周期第______族;氟在第_____周期第______族。
(2)写出下列物质的电子式:
氮气________;氯化镁_________;二氧化碳_______;氟化氢______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com