
| A. | C5H12 | B. | 甲苯的二氯代物 | C. | C6H14 | D. | C5H12O(醇类结构) |
分析 A.C5H12为戊烷,根据碳链异构来解答;
B.甲苯分子中的氢原子均可以被取代,发生二元取代,可以取代甲基上的2个H原子,可以取代甲基上1个H原子、苯环上1个H原子,也可以全部取代苯环上的2个H原子;
C.根据主链减碳作为取代基,利用碳链异构进行书写;
D.根据分子式为C5H12O的醇,书写戊基-C5H11异构体,戊基异构数目等于戊醇的异构体数目.
解答 解:A.戊烷的同分异构体有3种:正戊烷、异戊烷和新戊烷,结构简式分别为:CH3-CH2-CH2-CH2-CH3、 、
、 ;
;
B.若取代甲基上的2个H原子,有1种结构;
若取代甲基上1个H原子、苯环上1个H原子,则苯环上的Cl原子相对甲基有邻、间、对3种结构;
若全部取代苯环上的2个H原子,若其中1个Cl原子与甲基相邻,另一个Cl原子有如图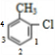 所示四种取代位置,有4种结构,若其中1个Cl原子处于甲基间位,另一个Cl原子有如图
所示四种取代位置,有4种结构,若其中1个Cl原子处于甲基间位,另一个Cl原子有如图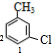 所示2种取代位置,有2种结构;
所示2种取代位置,有2种结构;
故甲苯的二氯代物共有1+3+4+2=10种;
C.C6H14属于烷烃,主链为6个碳原子有:CH3(CH2)4CH3;主链为5个碳原子有:CH3CH2CH2CH(CH3)2;CH3CH2CH(CH3)CH2CH3;主链为4个碳原子有:CH3CH2C(CH3)3;CH3CH(CH3)CH(CH3)CH3,则C6H14的同分异构体共有5种;
D.分子式为C5H12O的醇,戊基-C5H11可能的结构有:-CH2CH2CH2CH2CH3、-CH(CH3)CH2CH2CH3、-CH(CH2CH3)2、-CHCH(CH3)CH2CH3、-C(CH3)2CH2CH3、-C(CH3)CH(CH3)2、-CH2CH2CH(CH3)2、-CH2C(CH3)3,则戊醇的可能结构有8种;
所以同分异构体数目最多的是甲苯的二氯代物,
故选B.
点评 本题考查同分异构体的书写与判断,难度中等,注意二元取代采取定一移一法,注意重复、漏写.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作和现象 | 结论 |
| A | 室温下,向明矾溶液中溶液中加入足量的浓氨水 | 证明氢氧化铝溶于氨水 |
| B | 室温下,向浓度均为0.1mol•L-1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀. | Ksp(BaSO4)<Ksp(CaSO4) |
| C | 室温下,向硅酸钠溶液中通入足量的CO2出现白色沉淀. | 酸性:H2CO3>H2SiO3 |
| D | 室温下,用pH试纸测得:0.1mol•L-1 Na2SO3溶液的pH约为10;0.1mol•L-1 NaHSO3溶液的pH约为5. | HSO3-结合H+的能力比 SO32-的强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
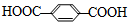 +nHOCH2CH2OH$\stackrel{一定条件}{→}$涤纶+(2n-1)H2O下列说法正确的是( )
+nHOCH2CH2OH$\stackrel{一定条件}{→}$涤纶+(2n-1)H2O下列说法正确的是( )| A. | 合成涤纶的反应为加聚反应 | |
| B. | 对苯二甲酸和苯甲酸互为同系物 | |
| C. | 1 mol涤纶与NaOH溶液反应,理论上最多可消耗2n mol NaOH | |
| D. | 涤纶的结构简式为: |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
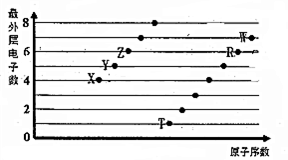 部分短周期元素原子最外层电子数与原子序数的关系如图,回答下列问题:
部分短周期元素原子最外层电子数与原子序数的关系如图,回答下列问题: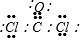 ;已知1mol XZW2与4mol NaOH
;已知1mol XZW2与4mol NaOH查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高a的反应温度,乙醇的转化率增大 | |
| B. | 由b可知:乙醇的燃烧热为13.8kJ•mol-1 | |
| C. | 对反应b来说,增大O2浓度可使△H2的值增大 | |
| D. | 以上两种途径,制取等量的氢气,无论哪种途径,消耗的能量均相同. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2的电子式: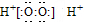 | |
| B. | 氮原子最外层电子轨道表达式: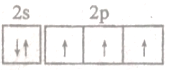 | |
| C. | Cl中子数为18的氯原子结构示意图: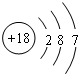 | |
| D. | 碳酸氢钠的电离方程式:NaHCO3?Na++H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
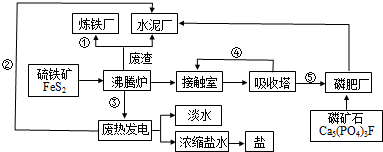
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制0.1mol/LNaCl溶液,定容时不小心加水超过刻度线,立即将水吸出 | |
| B. | 实验室制取氧气并用排水法收集,出现倒吸现象,立即停止加热 | |
| C. | 少量浓硫酸沾在皮肤上,立即用大量水冲洗,并涂上稀NaOH溶液 | |
| D. | 使用分液漏斗萃取碘水中的碘,振荡过程中要适时打开活塞进行“放气” |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com