
分子式为C3H6Cl2的同分异构体共有(不考虑立体异构)( )
A.3种 B.4种
C.5种 D.6种
科目:高中化学 来源: 题型:
原子序数为110的元素被发现后,它的符号被国际纯粹与应用化学联合会推荐为Ds(德语Darmstadt的缩写),以纪念该元素的发现地——德国。下列关于Ds的说法,不正确的是( )
A.Ds原子的电子层数为7
B.Ds是超铀元素
C.Ds原子的质量数为110
D.Ds为金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
糖类、油脂、蛋白质为动物性和植物性食物中的基本营养物质。下列说法正确的是( )
A.蛋白质中只含有C、H、O三种元素
B.油脂在人体中发生水解的产物是氨基酸
C.牛油、大豆油的主要成分都是高级脂肪酸甘油酯
D.糖类、油脂、蛋白质一定都能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法探究影响化学反应速率的因素。
实验一:利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1),设计实验方案,研究影响反应速率的因素。
(1)甲同学的实验报告如表所示:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取三份等体积的2 mol·L-1硫酸于试管中 ②分别投入大小、形状相同的Cu、Fe、Mg | 反应产生气泡的速率大小:Mg>Fe>Cu | 反应物的性质越活泼,反应速率越大 |
该同学的实验目的是__________________,要想得出正确的实验结论,还需要控制的实验条件是________________________________________________________________________。
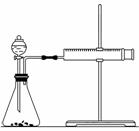
(2)乙同学为了能精确地研究浓度对反应速率的影响,在相同温度下利用如图所示装置进行定量实验。完成该实验应选用的实验药品是__________,应该测定的实验数据是____________。
实验二:已知2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在开始一段时间内反应速率较小,溶液褪色不明显,但反应一段时间后,溶液突然褪色,反应速率明显增大。
(3)针对上述实验现象,某同学认为该反应放热,导致溶液的温度升高,从而使反应速率增大。从影响化学反应速率的因素看,你认为还可能是________的影响。
(4)若要用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还可以在反应开始时加入________(填字母)。
A.硫酸钾 B.硫酸锰
C.氯化锰 D.水
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学欲在实验室中对Fe3+与I-的反应进行探究,实现Fe2+与Fe3+的相互转化。
(1)该同学最初的实验操作和现象如下:
| 编号 | 操作 | 现象 |
| Ⅰ | 先向2 mL 0.1 mol·L-1 FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 | |
| Ⅱ | 先向2 mL 0.1 mol·L-1 FeCl3溶液中滴加KSCN溶液,再滴加0.1 mol·L-1 KI溶液 | 滴加KSCN溶液后,溶液变成血红色;滴加KI溶液后,血红色无明显变化 |
①实验Ⅰ的现象为________________________________________________________________________。
②FeCl2溶液与新制氯水反应的离子方程式为________________________________________________________________________
________________________________________________________________________。
(2)该同学分析了导致实验Ⅱ现象的可能原因,并对实验方案进行了改进。改进后的实验操作和现象如下:
| 编号 | 操作 | 现象 |
| Ⅲ | 向2 mL 0.1 mol·L-1 KI溶液中滴加1 mL | |
| 0.1 mol·L-1 FeCl3溶液,再滴加KSCN溶液 | 滴加FeCl3溶液后,溶液变成黄色;滴加KSCN溶液后,溶液变成血红色 |
根据实验Ⅲ,该同学认为Fe3+有可能与I-发生氧化还原反应,请结合实验现象用简明的文字说明他得出上述结论的理由:________________________________________________________________________。
(3)该同学认为需要进一步设计实验,证明根据实验Ⅲ中现象得出的结论。请补全下表中的实验方案:
| 编号 | 操作 | 预期现象及结论 |
| Ⅳ | 向2 mL 0.1 mol·L-1 KI溶液中滴加1 mL0.1 mol·L-1 FeCl3溶液,__________ |
(4)上述实验结果表明,Fe3+有可能与I-发生氧化还原反应。进一步查阅资料知,参加反应的Fe3+与I-的物质的量相同。该同学结合上述实验结论,分析了实验Ⅲ中加入KSCN后溶液变血红的原因,认为Fe3+与I-反应的离子方程式应写为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有一类组成最简单的有机硅化合物叫硅烷。硅烷的组成、结构与相应的烷烃相似。
(1)写出硅烷分子式通式________________________________;
(2)写出乙硅烷在空气中自燃的化学方程式:_________________________________________________________________________________________________________________________________;
(3)相同状况下,甲硅烷的密度________(填“大于”“小于”或“等于”)甲烷;
(4)甲硅烷的热稳定性________(填“大于”“小于”或“等于”)甲烷。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.含有共价键的化合物一定是共价化合物
B.分子中只有共价键的化合物一定是共价化合物
C.由共价键形成的分子一定是共价化合物
D.只有非金属原子间才能形成共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
反应X(g)+Y(g)2Z(g) ΔH<0,达到平衡时,下列说法正确的是 ( )
A.减小容器体积,平衡向右移动
B.加入催化剂,Z的产率增大
C.增大c(X),X的转化率增大
D.降低温度,Y的转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com