
某兴趣小组的学生根据活泼金属Mg与CO2发生反应,推测活泼金属钠也能与CO2发生反应,因此兴趣小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去).已知:常温下,CO能使一些化合物中的金属离子还原
例如:PdCl2+CO+H2O=Pd↓+CO2+2HCl.反应生成黑色的金属钯,此反应也可用来检测微量CO的存在.
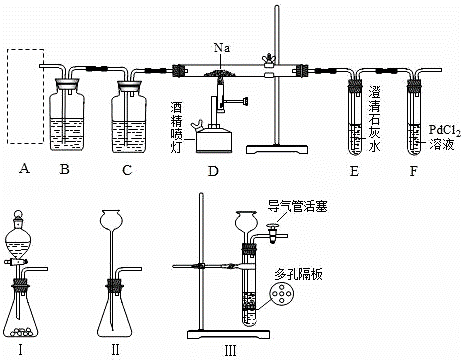
请回答下列问题:
(1)通常实验室制取CO2气体的离子方程式是,为了使制气装置能“随开随用,随关随停”,上图A处应选用的装置是Ⅲ(填写“Ⅰ”、“Ⅱ”或“Ⅲ”).若要制取干燥、纯净的CO2气体,装置B、C中各盛放的试剂分别为饱和、.
(2)装入药品后,在点燃酒精喷灯前,必须进行的操作是通.待装置填写字母)中出现浑浊现象时,再点燃酒精喷灯,这步操作的目的是.
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:
①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是.
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式(需注明正确的反应条件)是.
(4)请用文字简要说明你判断②中D装置生成固体的成分是钠的正盐还是酸式盐生成正盐理由:.
考点: 性质实验方案的设计.
专题: 实验设计题.
分析: (1)实验室常用碳酸钙与稀盐酸反应制取二氧化碳,制取气体的装置能“随开随用,随关随停”,是利用的启普发生器原理分析选择装置,制得的二氧化碳中含有氯化氢和水蒸气,利用装置B除氯化氢,利用装置C除水蒸气;
(2)为避免空气的影响,实验前先通二氧化碳充满装置后,再点燃酒精喷灯;
(3)①装置F中无明显现象,证明没有CO生成,装置D中残留固体(有两种物质)加盐酸有能使石灰水变浑浊的气体放出,其中一种固体为碳酸钠,另一种固体为C;
②装置D中的残留固体(只有一种物质)加盐酸有能使石灰水变浑浊的气体放出,说明生成碳酸钠,装置F中有黑色沉淀,说明PdCl2溶液能被CO还原得到黑色的Pd,所以反应产物为碳酸钠和CO;
(4)根据反应物的成分和质量守恒解答.
解答: 解:(1)实验室常用碳酸钙与稀盐酸反应制取二氧化碳,反应方程式为:CaCO3+2H+=Ca2++H2O+CO2↑;制取气体的装置能“随开随用,随关随停”,是利用的启普发生器原理分析选择装置;制得的二氧化碳中含有氯化氢和水蒸气,利用装置B饱和NaHCO3除氯化氢,利用装置C浓H2SO4除水蒸气;
故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;Ⅲ;饱和NaHCO3;浓H2SO4;
(2)为了避免空气中氧气、水蒸气影响探究二氧化碳和钠反应的产物分析,需要先把装置中空气排出,所以打开Ⅲ的导气管活塞,先通一会CO2气体,使装置充满二氧化碳气体后再点燃酒精喷灯;
故答案为:打开Ⅲ的导气管活塞,先通一会CO2气体;E;浑浊;排出该装置中的空气,避免空气中氧气、水蒸气影响探究二氧化碳和钠反应;
(3)①装置F中无明显现象,证明没有CO生成,装置D中残留固体(有两种物质)加盐酸有能使石灰水变浑浊的气体放出,
其中一种固体为碳酸钠,另一种固体为C,反应的方程式为4Na+3CO2 2Na2CO3+C;
2Na2CO3+C;
故答案为:4Na+3CO2 2Na2CO3+C;
2Na2CO3+C;
②由题意可知,装置D中的残留固体(只有一种物质)加盐酸有能使石灰水变浑浊的气体放出,说明生成碳酸钠,
装置F中有黑色沉淀,说明PdCl2溶液能被CO还原得到黑色的Pd,所以反应产物为碳酸钠和CO,反应的化学方程式为2Na+2CO2 Na2CO3+CO;
Na2CO3+CO;
故答案为:2Na+2CO2 Na2CO3+CO;
Na2CO3+CO;
(4)根据质量守恒定律可知,反应物CO2和Na中共有三种元素,没有氢元素,因此不能生成酸式盐,只能生成正盐;
故答案为:生成正盐;因为根据质量守恒定律可知,反应物共有三种元素,没有氢元素,因此不能生成酸式盐.
点评: 本题考查了实验装置的选择,物质性质的实验设计验证分析应用,主要是钠及其化合物性质的判断理解,掌握基础是关键,题目难度中等.


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
反应4NH3+5O2⇌4NO+6H2O在一定体积的密闭容器中进行,30s后NO的物质的量浓度增加了3mol/L,则下列反应速率正确的是()
A. v(NO)=0.1 mol•(L•s)﹣1 B. v(NO)=0.02 mol•(L•s)﹣1
C. v(NH3)=0.01 mol•(L•s)﹣1 D. v(NH3)=0.2 mol•(L•s)﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
下表标出的是元素周期表的一部分元素,回答下列问题:
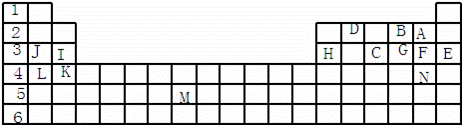
(1)表中用字母标出的14种元素中,化学性质最不活泼的是(用元素符号表示,下同),主族元素中金属性最强的是,非金属性最强是常温下单质为液态的非金属元素是;属于过渡元素的是(该空用字母表示).
(2)B、F、C气态氢化物的化学式分别为,其中以最不稳定.
(3)第三周期中原子半径最小的是.
查看答案和解析>>
科目:高中化学 来源: 题型:
有关下列实验操作和相应的离子方程式的说法正确的是()
A. 等物质的量MgCl2、Ba(OH)2和HCl溶液混合:Mg2++3OH﹣+H+=Mg(OH)2↓+H2O
B. Ca(HCO3)2溶液与过量NaOH溶液反应:Ca2++HCO3﹣+OH﹣=CaCO3↓+2H2O
C. 等物质的量的FeBr2与Cl2反应为:2Fe2++2Br﹣+2Cl2=2Fe3++Br2+4Cl﹣
D. 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4﹣+6H++5H2O2=2Mn2++5O2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl﹣、SO42﹣、CO32﹣、AlO2﹣ 中的若干种离子,离子浓度均为0.1mol•L﹣1.某同学进行了如下实验:

下列说法正确的是()
A. 无法确定原试液中是否含有Al3+、Cl﹣
B. 滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+
C. 无法确定沉淀C的成分
D. 原溶液中存在的离子为NH4+、Fe2+、Cl﹣、SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是一套实验室制气装置,用于发生、干燥和收集气体. 下列各组物质中能利用这套装置进行实验的是()

A. 铜屑和浓硝酸 B. 二氧化锰和浓盐酸
C. 锌和稀硫酸 D. 碳酸钙和稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,B、C、D同周期,A、D同主族,E与其它元素既不在同周期也不在同主族,B、C、D的最高价氧化物的水化物两两混合均能发生反应.D的单质为淡黄色固体.根据以上信息,回答下列问题:
(1)A和D的氢化物中,稳定性较弱的是D(填A或D);
(2)元素C在元素周期表中的位置是第周期、族.
(3)E元素的名称是钙.其离子结构示意图.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验仪器中,常用于物质分离的是( )
①容量瓶 ②漏斗 ③试管夹 ④蒸馏烧瓶 ⑤分液漏斗 ⑥滴管.
|
| A. | ①④⑤ | B. | ②④⑤ | C. | ③④⑥ | D. | ①②⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com