
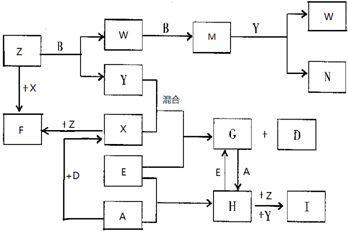
���� A��B��C��D�Ƕ�����Ԫ�ص���̬���ʣ�����A�ǻ���ɫ�����嵥�ʣ���AΪCl2��C�ڿ����к�����ߣ���CΪN2��D����������壬��DΪH2��E��һ����õĽ�������EΪFe��Y��һ�ֳ�����Һ̬���ʣ���YΪH2O��Z��Ψһ�Լ��Ե����壬��ZΪNH3��M��һ�ֺ���ɫ���ж����壬��MΪNO2��IΪ���ɫ������ˮ�Ĺ��壬��IΪ2Fe��OH��3�����ݸ����ʵ��ת����ϵ��֪��Z��B��Ӧ����W��Y����BΪO2��W����������M����WΪNO������������ˮ��Ӧ����NΪ���ᣬA��D��Ӧ����XΪHCl���Ȼ����백����Ӧ����FΪNH4Cl������������Ӧ����HΪFeCl3����GΪFeCl2���ݴ˴��⣮
��� �⣺A��B��C��D�Ƕ�����Ԫ�ص���̬���ʣ�����A�ǻ���ɫ�����嵥�ʣ���AΪCl2��C�ڿ����к�����ߣ���CΪN2��D����������壬��DΪH2��E��һ����õĽ�������EΪFe��Y��һ�ֳ�����Һ̬���ʣ���YΪH2O��Z��Ψһ�Լ��Ե����壬��ZΪNH3��M��һ�ֺ���ɫ���ж����壬��MΪNO2��IΪ���ɫ������ˮ�Ĺ��壬��IΪ2Fe��OH��3�����ݸ����ʵ��ת����ϵ��֪��Z��B��Ӧ����W��Y����BΪO2��W����������M����WΪNO������������ˮ��Ӧ����NΪ���ᣬA��D��Ӧ����XΪHCl���Ȼ����백����Ӧ����FΪNH4Cl������������Ӧ����HΪFeCl3����GΪFeCl2��
��1��AΪCl2��A�����Ԫ����Ԫ�����ڱ���λ��Ϊ�������ڵ�VIIA�壬
�ʴ�Ϊ���������ڵ�VIIA�壻
��2��FΪNH4Cl��F�л�ѧ�������������Ӽ��������ԣ����ۼ���
�ʴ�Ϊ�����Ӽ��������ԣ����ۼ���
��3��Z��W�ڴ��������·�Ӧ����C��Y��Ϊ������һ�������ķ�Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ 4NH3+6NO $\frac{\underline{����}}{��}$5N2+6 H2O��
�ʴ�Ϊ��4NH3+6NO $\frac{\underline{����}}{��}$5N2+6 H2O��
��4��IΪ2Fe��OH��3��I�롰84����Һ������Ч�ɷ֣�NaClO������Ũ����Һ�з�����Ӧ�����˸�Ч�����ľ�ˮ���������ƣ��˷�Ӧ�����ӷ���ʽΪ2Fe��OH��3+3 ClO-+4OH-=2FeO42-+3 Cl-+5H2O��
�ʴ�Ϊ��2Fe��OH��3+3 ClO-+4OH-=2FeO42-+3 Cl-+5H2O��
��5�������������ӵ�ϡ������Һ�У���������������ÿĦ����ת��2mol���ӣ�������������ת�Ƶ��ӵ���ĿΪ3.01��1023��0.5mol����μӷ�Ӧ����������Ϊ56��$\frac{0.5}{2}$g=14g��
�ʴ�Ϊ��14��
���� ���⿼��Ԫ�ػ���������Ժͷ�Ӧ�����⿼�������ƶϣ����ʵ���ɫ������ЧӦ���塢�γ��������������ƶ�ͻ�ƿڣ���Ŀ�Ƚ��ۺϣ���Ҫѧ���������ջ���֪ʶ֪ʶ���Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ư���е���Ч�ɷ�Ϊ������ƣ��ڿ����п��Գ�ʱ����ö������� | |
| B�� | ���������ǽ�̫����ת��Ϊ���ܵij��ò��� | |
| C�� | ����ŦԼ�������й�ůʹ�õ���Ҫ��Դ����Ȼ������Ȼ�����ڲ���������Դ | |
| D�� | �����������õ��˴�������ʯ�ң�����ʯ��Ͷ�����̳صĺ�ˮ�У���ˮ��ʼ���ڣ�����һ�������仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 A��B��C��D��E��F �������ʵ�ת����ϵ��ͼ��ʾ����Ӧ�����Ͳ��ֲ���δ�������
A��B��C��D��E��F �������ʵ�ת����ϵ��ͼ��ʾ����Ӧ�����Ͳ��ֲ���δ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
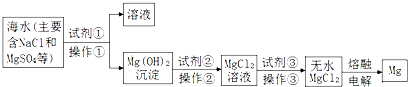
| A�� | �Լ��ٿ���ѡ�õ��Լ�����ʯ�ң������ٵķ����ǹ��� | |
| B�� | �Լ��ڿ���ѡ�õ��Լ������� | |
| C�� | ��������ֱ�ӽ�MgCl2��Һ���������õ���ˮMgCl2���� | |
| D�� | ��ˮMgCl2��ͨ��ʱ�������룬����õ�����Mg�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��10ml0.1mol/L��Ca��ClO��2����Һ�й����̬�µ�SO2����44.8ml��Ca2++2ClO-+2H2O+2SO2=CaSO4��+2Cl-+4H++SO42- | |
| B�� | ��98.3%��Ũ�����м���ͭƬ�����ȣ�Cu+4H++SO42-$\frac{\underline{\;\;��\;\;}}{\;}$SO2��+2H2O+Cu2+ | |
| C�� | ��NH4HCO3��Һ�м�����ŨNaOH��Һ�����ȣ�HCO3-+OH-$\frac{\underline{\;\;��\;\;}}{\;}$H2O+CO32- | |
| D�� | ���Ȼ�狀���ʯ�����ֹ����ϼ����ư�����NH4++OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֽ������ͨ������ֽ��Ϊ����֧�����ֽ��ά�ϵ��ǻ�������ˮ�ԣ�����������ˮ���̶��� | |
| B�� | �ؽᾧʱ�����ʵ��ܽ��Խ����Һ��ȴ�ٶ�Խ�����õ��ľ������ԽС | |
| C�� | ����ر�����Һ��ȴδ���ֽᾧʱ�������ò������ĥ������ڴ�ʹ�������� | |
| D�� | ������Ľ���Һ�м������Ƽ���Cu��OH��2����Һ�����ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
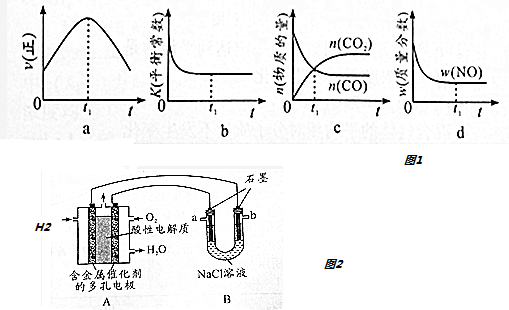
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
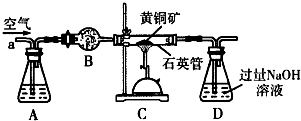

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ռ�������$\frac{22.4b}{2{N}_{A}}$L | |
| B�� | ��Ӧ����Һ�е�Cl-��ĿΪ��bc•NA-2d�� | |
| C�� | NA�ɱ�ʾΪ$\frac{87d}{2a}$ | |
| D�� | ��Ӧ����Һ�е�H+��ĿΪ��bc-2d�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com