
【题目】在无色溶液中,下列离子能大量共存的是( )
A.Mg2+、SO42-、K +、Cl-B.Na+ 、NH4+ 、NO3-、MnO4-
C.K + 、Cu2+ 、Cl-、Br-D.Ba2+ 、Na+ 、NO3-、CO32-
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】著名化学家徐光宪,因为在稀土萃取领域取得的卓越成就被誉为“稀土界的袁隆平”;2009 年,胡锦涛 主席为其颁发了“国家最高科学技术奖”。稀土元素是指镧系的 15 种元素,加上钪和钇共 17 种元素。下列 说法正确的是
A. 稀土元素全部是金属元素 B. 要萃取出碘酒中的碘可用 KOH 溶液做萃取剂
C. 镧系元素属于主族元素 D. 某些稀土元素在地壳中的含量高于铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在一容积不变的密闭容器中发生可逆反应2X(g)![]() Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是
Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是
A. 混合气体的密度不再变化 B. 反应容器中Y的质量分数不变
C. 体系压强不再变化 D. 2v逆(X)=v正(Y)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠离子电池正成为化学电源的新宠。
(1)有一种新型的高能电池—钠硫电池(熔融的钠、硫为两极,以Na+导电的βAl2O3陶瓷作固体电解质),反应式为2Na+xS ![]() Na2Sx。
Na2Sx。
①充电时,钠极与外电源________(填“正”或“负”)极相连。其阳极反应式:_____________。
②用该电池作电源电解(如图)NaCl溶液(足量),写出电解NaCl溶液的离子方程式:________________________________。

③若用该钠硫电池作电源在一铁片上镀铜,此铁片与__________(填“钠”或“硫”)极相连。
(2)“Na-CO2”电池可将CO2变废为宝。我国科研人员研制出的可充电“ Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2 ![]() 2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示:
2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示:

①放电时,正极的电极反应式为_____________________________。
②若生成的Na2CO3和C全部沉积在电极表面,当转移0.2 mol e-时,两极的质量差为________ g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色工业废水中可能含有Na+、Mg2+、Al3+、Cu2+、Cl-、SO42-中的几种离子。
a.取10 mL该废水于试管中,加入足量的Ba(NO3)2溶液和稀硝酸,产生白色沉淀,充分反应后过滤,向滤液中加入AgNO3溶液无沉淀产生。
b.另取10 mL该废水于试管中,滴加NaOH溶液先产生白色沉淀,后部分沉淀溶解,生成沉淀的物质的量随加入NaOH的物质的量关系如图所示。
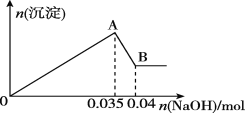
根据上述实验回答下列问题:
(1)该废水中一定不含有的离子有______________(填离子符号)
(2)实验室配制100 mL 1.0 mol·L-1的NaOH溶液时,用到的玻璃仪器除烧杯、玻璃棒、量筒外,还需要______________(填仪器名称)
(3)写出A→B过程中发生反应的离子方程式:______________
(4)该废水中,c(Al3+)=____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适量的铁粉加入FeCl3溶液中,完全反应后,溶液中的Fe3+和Fe2+的物质的量浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比( )
A.3︰2B.1︰2C.2︰1D.2︰3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表达下列反应的离子方程式为
A. NaHCO3溶液中加足量Ba(OH)2溶液:2HCO3-+Ba2++2OH-![]() BaCO3↓+CO32-+2H2O
BaCO3↓+CO32-+2H2O
B. 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO—![]() CaSO3↓+2HClO
CaSO3↓+2HClO
C. 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-![]() 2Mn2++10CO2↑+8H2O
2Mn2++10CO2↑+8H2O
D. 电解饱和食盐水获取烧碱和氯气: 2Cl—+ 2H2O![]() H2↑+ Cl2↑+2OH—
H2↑+ Cl2↑+2OH—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com