
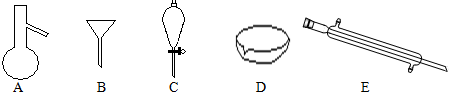
分析 (1)图中A是蒸馏烧瓶、B为漏斗、C是分液漏斗、D为蒸发皿、E是冷凝管;
(2)泥沙不溶于水,而粗盐溶于水;花生油和水混合分层;
(3)A.A仪器需要垫石棉网加热;
B.利用漏斗向酒精灯中添加酒精;
C.分液时应打开上边的瓶塞,利用气压使液体流下;
D.蒸发要不断用玻璃棒搅拌;
E.E仪器中水的流向是下进上出;
(4)四氯化碳和水不互溶,且碘在四氯化碳中的溶解度大于水中的溶解度.
解答 解:(1)图中C是分液漏斗、E是冷凝管,故答案为:分液漏斗;冷凝管;
②泥沙不溶于水,而粗盐溶于水,需要过滤分离,则选择B漏斗;花生油和水混合分层,则需要分液法分离,选择C仪器,故答案为:B;C;
(3)A.A仪器需要垫石棉网加热,不能直接利用酒精灯加热,故A错误;
B.利用漏斗向酒精灯中添加酒精,可防止酒精滴落或发生意外,故B正确;
C.分液时应打开上边的瓶塞,平衡气压,利用气压使液体流下,故C正确;
D.蒸发要不断用玻璃棒搅拌,防止局部温度过高,导致液体飞溅,故D正确;
E.E仪器中水的流向是下进上出,在冷凝管中的停留时间长,冷却效果好,故E错误;
故答案为:BCD;
(4)四氯化碳能萃取碘水中的碘,但密度大于水的密度,看到的现象是溶液分层,碘溶解于四氯化碳中呈紫红色,所以下层呈紫红色,上层是水层,呈无色,
故答案为:分液漏斗内液体分两层,上层液体无色,下层液体紫红色.
点评 本题考查混合物分离提纯,为高频考点,把握仪器的使用、混合物分离提纯方法及原理等为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 36:60 | B. | 60:36 | C. | 1:2 | D. | 1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 依据氧化还原反应:
依据氧化还原反应:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
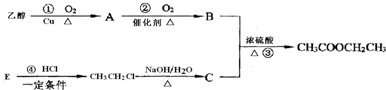
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
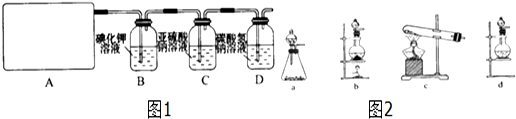
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入苯使之反应 | B. | 加入KI溶液 | ||
| C. | 加入较大量NaOH溶液后静置分液 | D. | 加入较大量的CCl4萃取静置后分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com