
(10分)A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处在同一周期,A、C处在同一主族。C原子核内质子数等于A、B原子核内质子数之和,C原子最外层上的电子数是D原子最外层电子数的4倍。试回答:
(1)写出下列元素的元素名称:A________,B________,C________,D________。
(2)这四种元素中在常温常压下的液态或气态氢化物的稳定性由大而小的顺序是________。
(3)A与B形成的三原子分子的电子式是________,B与D形成的原子个数比为1∶1的化合物的电子式是________。
(4)A元素某氧化物与D元素某氧化物反应生成单质的化学方程式是______________________。
(1)碳 氧 硅 钠 (各1分) (2)H2O>CH4>SiH4 (2分)
(3)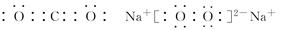 (各1分)
(各1分)
(4)2CO2+2Na2O2=2Na2CO3+O2 (2分)
解析试题分析:A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处在同一周期,A、C处在同一主族,四种元素在周期表中的大致相对位置为: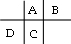 ,A、C处在同一主族,二者质子数相差8,C原子核内质子数等于A、B原子核内质子数之和,故B的质子数为8,B为O元素,C原子最外层上的电子数是D原子最外层电子数的4倍,故C最外层电子数为4,D的最外层电子数为1,故A为C元素,C为Si元素,D为Na元素,则
,A、C处在同一主族,二者质子数相差8,C原子核内质子数等于A、B原子核内质子数之和,故B的质子数为8,B为O元素,C原子最外层上的电子数是D原子最外层电子数的4倍,故C最外层电子数为4,D的最外层电子数为1,故A为C元素,C为Si元素,D为Na元素,则
(1)根据以上分析可知四种元素名称分别为碳、氧、硅、钠。
(2)非金属性越强,氢化物的稳定性越强,非金属性是O>C>Si,所以氢化物的稳定性由大而小的顺序是H2O>CH4>SiH4。
(3)碳与氧形成的三原子分子是二氧化碳,其电子式是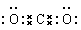 ;钠与氧形成的原子个数比为1∶1的化合物是过氧化钠,其电子式是
;钠与氧形成的原子个数比为1∶1的化合物是过氧化钠,其电子式是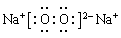 。
。
(4)二氧化碳能与过氧化钠反应生成氧气和碳酸钠,反应的方程式为2CO2+2Na2O2=2Na2CO3+O2。
考点:考查位置、结构与性质应用的有关判断


科目:高中化学 来源: 题型:单选题
下列说法中不正确的是 ( )
①质子数相同的粒子一定属于同一种元素
②同位素的性质几乎相同
③质子数相同,电子数也相同的粒子,不可能是一种分子和一种离子
④电子数相同的粒子不一定是同一种元素
⑤一种元素只能有一种质量数
⑥某种元素的相对原子质量取整数,就是其质量数
| A.②④⑤⑥ | B.①②④⑤ | C.①②⑤⑥ | D.③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A、B、C为三种短周期元素,A、B同周期,A、C的最低价离子分别为A2-、C-,B2+与C-具有相同的电子层结构,下列叙述一定不正确的是
A.离子半径A2->C->B2+
B.它们的原子半径C>B>A
C.它们的原子序数A>B>C
D.原子最外层上的电子数C>A>B
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
1907年2月2日,享誉世界的俄国化学家门捷列夫因心肌梗塞与世长辞,那一天距离他的73岁生日只有六天。门捷列夫在科学界的主要贡献是
| A.发现色盲现象 | B.发现元素周期律 |
| C.发明硝酸甘油炸药 | D.发现了放射性元素钋 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
| A.元素原子的最外层电子数等于元素的最高化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
| D.Na、Mg、Al失电子能力和最高价氧化物对应水化物的碱性均依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(9分)已知A、B、C、D、E、F都是短周期的主族元素,原子序数依次增大,其中A是宇宙中最丰富的元素,B的单质常温下为气体,C和E同主族,C和E可形成EC2和EC3两种分子,D是短周期中原子半径最大的元素。请回答下列问题:
(1)①B在元素周期表中的位置________________________________;
②上述元素的最高价氧化物的水化物中酸性最强的是 (写化学式)。
(2)C、D、E、F四种元素对应的简单离子的半径由小到大的顺序是(用离子符号表示) 。
(3)工业上常用A、B组成的物质X来检验F的单质是否发生泄漏,有大量白烟生成,写出此反应的化学方程式____________。其中该反应中还原剂和氧化剂的物质的量之比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(每空2分,共12分)下图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格: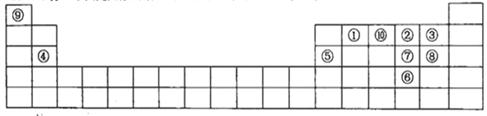
(1)在这10种元素中,非金属性最强的是___________(填序号);
(2)元素②⑧⑨以原子个数比1:1:1形成的化合物的结构式为______________________,元素②与⑨形成的18e-化合物的电子式____________________;
(3)②、⑨、⑩三种元素形成的化合物M中原子个数比为3:4:2,电子总数为42,M中含有的化学键类型有___________________________;
(4)比较元素⑦⑧形成的气态氢化物的稳定性:____>____(用化学式表示)
(5)元素⑤的氧化物与氢氧化钠溶液反应的离子方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(18分)(1)按已知的原子结构规律,82号元素X应是第___________周期_________族元素,它的最高正价氧化物的化学式为______________。
(2)以下反应:①木炭与水制备水煤气 ②氯酸钾分解 ③炸药爆炸 ④酸与碱的中和反应 ⑤生石灰与水作用制熟石灰 ⑥ Ba(OH)2·8H2O与NH4Cl,属于放热反应_____________填序号),写出反应⑥的化学方程式__ ____。
(3)在下列化合物中:H2O2 、Na2O、、I2 、、NaCl、、CO2、NH4Cl、Na2O2,用化学式回答下列问题:
①只由非金属组成的离子化合物是 ,②只有极性共价键的共价化合物是 ,
③只含有非极性共价键的是 ,④既有离子键又有非极性键的化合物是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
M是原子序数<30的一种金属,常用于航空、宇航、电器及仪表等工业部门,M原子的最外层有空轨道,且有两个能级处于电子半充满状态。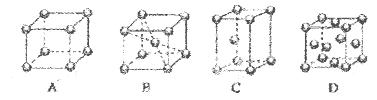
(1)M原子的外围电子排布式为_______________,在周期表中属于___________区元素。
(2)M的堆积方式属于钾型,其晶胞示意图为____(填序号)。其空间利用率为____。
(3) MCl3?6H2O有三种不同颜色的异构体
A、[M(H2O)6]Cl3,B、[M(H2O)5Cl]Cl2?H2O和C、[M(H2O)4Cl2]Cl?2H2O
为测定蒸发MCl3溶液析出的暗绿色晶体是哪种异构体,取0.10molMCl3·6H2O 配成溶液,滴加足量AgNO3溶液,得到沉淀2.870 g。该异构体为___________(填A或B或C)。
(4)常温下为暗红色液体,熔点-96. 5℃,沸点117℃,能与丙酮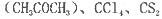 等互溶。
等互溶。
①固态MO2Cl2属于___________晶体;
②中碳原子和丙酮(CH3COCH3)羰基中的碳原子分别采取的杂化方式为______杂化和_____杂化。
(5)+3价M的配合物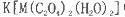 中,配体是___________,与C2O42-互为等电子体的分子是(填化学式)_______________。
中,配体是___________,与C2O42-互为等电子体的分子是(填化学式)_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com