
| A.5~9 | B.4.0~10.0 | C.4.3~9.7 | D.以上都不正确 |
 mol/L
mol/L



 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.向洗涤液中滴加碳酸钠溶液可检验沉淀是否洗涤干净 |
| B.上述变化过程中包括了分解、化合、复分解、置换等四种反应类型 |
| C.在氯化氢热气流中干燥晶体的目的是为了加快干燥速度 |
| D.步骤⑤也可以采用电解该盐水溶液的方法 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.称取7.68g硫酸铜,加入500mL水 | B.称取12.0g胆矾配成500mL溶液 |
| C.称取8.0g硫酸铜,加入500mL水 | D.称取12.5g胆矾配成500mL溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
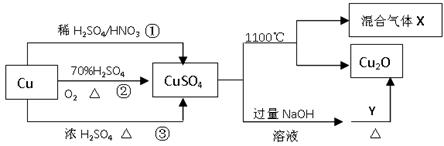
| A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3∶2 |
| B.相对于途径①、③,途径②更好地体现了绿色化学思想 |
| C.1molCuSO4在1100℃所得混合气体X中O2一定为0.75mol |
| D.Y可以是葡萄糖 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
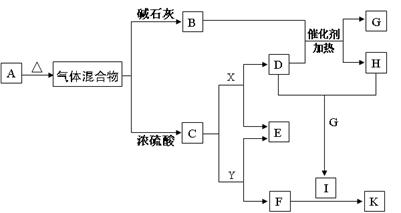
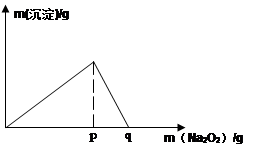
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 KMnO4 + H2C2O4 + ( )---K2SO4 + CO2↑+ MnSO4 + ( )
KMnO4 + H2C2O4 + ( )---K2SO4 + CO2↑+ MnSO4 + ( )查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.试样中含有加热不挥发的杂质 |
| B.试样中含有加热易挥发的杂质 |
| C.测试前试样已有部分脱水 |
| D.实验前坩埚未完全干燥 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
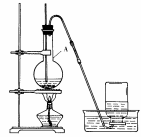
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
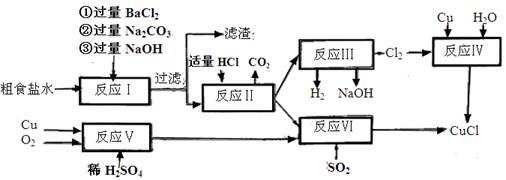
 。
。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com