
| A. | NaOH是氧化产物 | B. | 该反应电子转移数为2e- | ||
| C. | NaH为还原剂 | D. | H2O既是还原剂又是氧化剂 |
分析 NaH+H2O═NaOH+H2↑中,NaH中H元素的化合价由-1价升高为0,H2O中H元素的化合价由+1价降低为0,以此解答.
解答 解:NaH+H2O═NaOH+H2↑中,NaH中H元素的化合价由-1价升高为0,H2O中H元素的化合价由+1价降低为0,
A.反应中只有H元素的化合价变化,则氢气既是还原产物又是氧产物,故A错误;
B.NaH+H2O═NaOH+H2↑中,NaH中H元素的化合价由-1价升高为0,H2O中H元素的化合价由+1价降低为0,则该反应转移电子数为1e-,故B错误;
C.在NaH中H元素的化合价由-1价升高为0,NaH为还原剂,故C正确;
D.NaH为还原剂,水为氧化剂,故D错误;
故选C.
点评 本题考查氧化还原反应,明确反应中元素的化合价变化是解答本题的关键,注意NaH中H为负价,题目难度不大.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:解答题
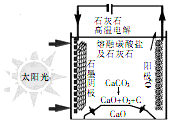 二氧化碳被认为是加剧温室效应的主要物质,资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品.
二氧化碳被认为是加剧温室效应的主要物质,资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品.| 选项 | CO | H2 | CH4 | H2O |
| A | 0 | 0 | 1 | 2 |
| B | 2 | 8 | 0 | 0 |
| C | 1 | 4 | 1 | .2 |
| D | 0.5 | 2 | 0.5 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
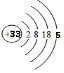 .
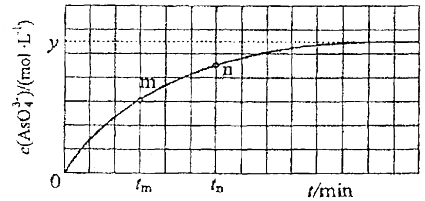
.
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙烯和聚氯乙烯都能使溴的四氯化碳溶液褪色 | |
| B. | 乙烷、丙烷、丁烷都没有同分异构体 | |
| C. | 酒越陈越香与酯化反应有关 | |
| D. | 甲烷与足量氯气在光照下反应可生成难溶于水的油状液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | |||
| Z | W | Y |
| A. | Y的气态氢化物比X的氢化物沸点低 | |
| B. | Z元素的氧化物属于碱性氧化物 | |
| C. | 原子半径由小到大的顺序为:X<Z<Y<W | |
| D. | Y元素最高价氧化物对应的水化物化学式为H3YO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氰分子中四原子共直线,是非极性分子 | |
| B. | 氰分子中C≡N键长大于C≡C键长 | |
| C. | 氰气分子中含有σ键和π键 | |
| D. | 氰化氢在一定条件下能与烯烃发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径:Z>W>X>Y | |
| B. | W、X形成的化合物中一定含有离子键 | |
| C. | 最简单氢化物的还原性:Z>W | |
| D. | 工业上常用电解熔融氯化物的方法制备X、Y的单质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com