
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源:不详 题型:单选题
| A.在多电子的原子里,能量高的电子通常在离核近的区域内活动 |
| B.核外电子总是先排在能量低的电子层上,例如只有排满了K层后才排L层 |
| C.两种微粒,若核外电子排布完全相同,则其化学性质一定相同 |
| D.微粒的最外层只能是8个电子才稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②④ | B.②③④ | C.③④⑥ | D.①⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.A形成 +1价阳离子 | B.Z一定能与水反应 |
| C.Z中只能含有离子键 | D.Z的熔点较高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
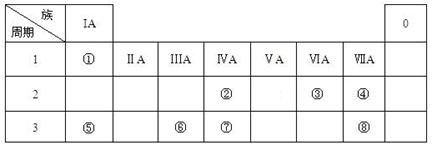
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 原子 | N | S | O | Si |
| 半径r/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在空气中燃烧都能生成过氧化物 | B.都能够与水反应 |
| C.都有较强的还原性 | D.最高价氧化物对应水化物都是强碱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com