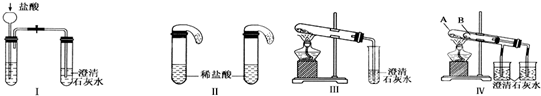
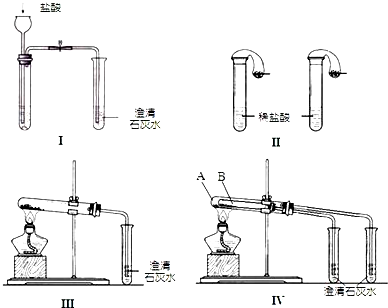
解:(1)无论碳酸钠还是碳酸氢钠都能和盐酸反应生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊,故Ⅰ无法鉴别;
实验Ⅱ中,盐酸和碳酸氢钠反应立即产生气泡,盐酸和碳酸钠先反应生成碳酸氢钠,碳酸氢钠和盐酸反应生成二氧化碳气体,所以看到的现象不同,故能鉴别碳酸钠和碳酸氢钠.
故答案为:Ⅱ.
(2)①碳酸氢钠在加热条件下能分解生成碳酸钠、水和二氧化碳2NaHCO
3
Na
2CO
3+H
2O+CO
2↑.
②Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行,故选D.
故答案为:2NaHCO
3
Na
2CO
3+H
2O+CO
2↑;D.
(3)碳酸钠直接加热,碳酸氢钠不直接加热,不直接加热的碳酸氢钠能分解而直接加热的碳酸钠不分解更能说明碳酸氢钠不稳定.
故答案为:NaHCO
3.
(4)碳酸氢钠与氢氧化钙的物质的量之比为2:1时,反应方程式为
2NaHCO
3+Ca(OH)
2=CaCO
3↓+Na
2CO
3+2H
2O,根据方程式知该溶液是碳酸钠溶液;该溶液中含有碳酸根离子,碳酸根离子能和钙离子生成白色沉淀,所以检验方法是:取上层清液于洁净的试管中加入适量CaCl
2溶液,振荡,若有白色沉淀生成,则证明溶液中含有CO
32-.
故答案为:Na
2CO
3;取上层清液于洁净的试管中加入适量CaCl
2溶液,振荡,若有白色沉淀生成,则证明溶液中含有CO
32-.
(5)加热固体,能使澄清石灰水变浑浊固体是碳酸氢钠,不能使澄清石灰水变浑浊的是碳酸钠,2NaHCO
3
Na
2CO
3+H
2O+CO
2↑.
故答案为:加热固体,能使澄清石灰水变浑浊固体是碳酸氢钠,不能使澄清石灰水变浑浊的是碳酸钠,
2NaHCO
3
Na
2CO
3+H
2O+CO
2↑.
分析:(1)根据实验现象是否有明显区别判断.
(2)①碳酸氢钠不稳定,在加热条件下能分解生成碳酸钠、二氧化碳和水,碳酸钠较稳定,加热不易分解.
②根据是否有对比性判断.
(3)不直接加热碳酸氢钠就能分解更说明碳酸氢钠不稳定.
(4)根据反应方程式判断溶液中的溶质;碳酸根离子能和钙离子反应生成碳酸钙白色沉淀,向上层清液中加入氯化钙溶液,若产生白色沉淀,就证明有碳酸根离子.
(5)根据碳酸钠和碳酸氢钠性质的不同设计实验.
点评:本题考查了碳酸钠和碳酸氢钠的性质,难度较大的是实验设计,要根据物质的性质来设计实验,检验物质的性质.


 Na2CO3+H2O+CO2↑.
Na2CO3+H2O+CO2↑. Na2CO3+H2O+CO2↑;D.
Na2CO3+H2O+CO2↑;D. Na2CO3+H2O+CO2↑.
Na2CO3+H2O+CO2↑. Na2CO3+H2O+CO2↑.
Na2CO3+H2O+CO2↑.

 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案 某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示.
某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示.