
下列溶液中Cl-的物质的量浓度最大的是( )
| A.200mL 2mol/L MgCl2溶液 | B.1000mL 2.5mol/L NaCl溶液 |
| C.250mL 1mol/L AlCl3溶液 | D.300mL 5mol/L KClO3溶液 |
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:阅读理解
| 实验方法 | 实验现象 | 结论 |
| 在溶液中加入KSCN溶液 | 溶液变血红色 溶液变血红色 |
固体物质中有FeCl3 |
| 在酸性KMnO4溶液中加入少量A | KMnO4溶液颜色无明显变化 | 固体物质中不含 FeCl2 FeCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
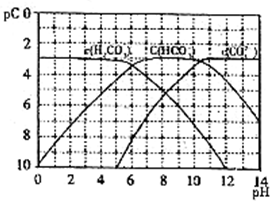 pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为1×10-3mol/L,则溶液中该溶质的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡:
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为1×10-3mol/L,则溶液中该溶质的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡:| O | - 3 |
| O | - 3 |
| O | 2- 3 |
| O | - 3 |
| O | 2- 3 |
| O | 2- 3 |
| O | - 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中含有丰富的镁资源.某同学设计了从模拟海水中制备MgO的实验方案:
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2010年东北三省联考高考化学一模试卷(解析版) 题型:解答题
 pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为1×10-3mol/L,则溶液中该溶质的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡:
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为1×10-3mol/L,则溶液中该溶质的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡:
 ?
?
 、
、 在加入强酸或强碱溶液后,平衡时溶液中三种成分的pC-pH图.请回答下列问题:
在加入强酸或强碱溶液后,平衡时溶液中三种成分的pC-pH图.请回答下列问题: 的pC最大值为______(溶液中的离子浓度小于1×10-5mol/L时,沉定完全).
的pC最大值为______(溶液中的离子浓度小于1×10-5mol/L时,沉定完全). 的物质的量之比为2:1,则滴入的盐酸中HCl的物质的量等于______mol.
的物质的量之比为2:1,则滴入的盐酸中HCl的物质的量等于______mol.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com