
| A. | 通过煤的气化和液化获得洁净的燃料 | |
| B. | 加快核能、太阳能、沼气等新能源的开发利用 | |
| C. | 减少资源消耗,注重资源的重复使用、资源的循环再生 | |
| D. | 大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 |
分析 核能、太阳能、风能为清洁能源,煤的气化和液化、大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源,可减少化石能源的使用,减少环境污染,以此解答该题.
解答 解:A.煤的气化和液化可以去除煤中的硫,可以防止燃烧生成二氧化碳污染空气,所以煤的气化和液化是使煤变成清洁能源的有效途径,故A正确;
B.沼气不是新能源,新能源是指在新技术的基础上系统开发利用的能源,如太阳能、风能、生物质能、地热能、海洋能、核能、氢能等,故B错误;
C.减少资源消耗,注重资源的重复使用、资源的循环再生,可有效利用资源,故C正确;
D.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源,可充分利用资源,减少垃圾污染,故D正确.
故选B.
点评 本题综合考查化学反应与能量变化,为高频考点,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,提高学习的积极性,注意相关基础知识的积累.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(g)(△H<0)
在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(g)(△H<0)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
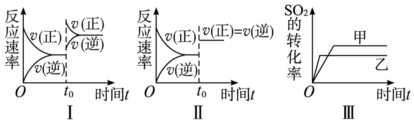
| A. | 图Ⅰ研究的是t0时刻增大O2的浓度对反应速率的影响 | |
| B. | 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较低 | |
| C. | 图Ⅲ研究的是催化剂对平衡的影响,且甲的催化效率比乙高 | |
| D. | 图Ⅱ研究的是t0时刻加入催化剂后对反应速率的影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | △H>0表示产物的总能量低于反应物的总能量 | |
| C. | △H 的单位kJ•mol-1,热量Q的单位为kJ | |
| D. | 化学键断裂过程中释放能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(B2-)+c(HB-)=0.1 mol/L | B. | c(B2-)+c(HB-)+c(H2B)=0.1 mol/L | ||
| C. | c(OH-)=c(H+)+c(HB-)+2c(H2B) | D. | c(Na+)+c(OH-)=c(H+)+c(HB-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{44}$ mol-1 | B. | $\frac{x}{22}$ mol-1 | C. | $\frac{3x}{44}$ mol-1 | D. | $\frac{44x}{3}$ mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解质不一定能导电 | |
| B. | 氨溶于水得到的氨水能导电,所以氨水是电解质 | |
| C. | 将硫酸钡放入水中不能导电,所以硫酸钡是非电解质 | |
| D. | 在水溶液或熔融状态下能导电的物质叫做电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com