
| A. | 44 g CO2 气体中含有原子数为2NA | |
| B. | 常温常压下22.4 L H2 中含原子数为2NA | |
| C. | 64g二氧化硫含有原子数为3NA | |
| D. | 标准状况下22.4 L H2O中含分子数为NA |
分析 A、求出二氧化碳的物质的量,然后根据二氧化碳为三原子分子来分析;
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、求出二氧化硫的物质的量,然后根据二氧化硫为三原子分子来分析;
D、标况下水为液态.
解答 解:A、44g二氧化碳的物质的量为1mol,而二氧化碳为三原子分子,故1mol二氧化碳中含3NA个原子,故A错误;
B、常温常压下,气体摩尔体积大于22.4L/mol,故22.4L氢气的物质的量小于1mol,则含有的原子数小于2NA个,故B错误;
C、64g二氧化硫的物质的量为1mol,而二氧化硫为三原子分子,故1mol二氧化硫中含3NA个原子,故C正确;
D、标况下水为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题
| X | Y | |
| Z | W |
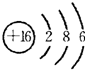 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | X | |
| Y | Z |
| A. | X、Y、Z中最简单氢化物稳定性最弱的是Y | |
| B. | Z元素氧化物对应水化物的酸性一定强于Y | |
| C. | X元素形成的单核阴离子还原性强于Y | |
| D. | Z元素单质在化学反应中只表现氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:rW>rZ>rY | |
| B. | 化合物X2Y、ZY、ZX2中化学键的类型相同 | |
| C. | 由X、Y、Z、W组成的化合物的水溶液可能显酸性 | |
| D. | 由Y元素形成的离子与W元素形成的离子的电子数不可能相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 4Z | B. | 4Z+6 | C. | 4Z+10 | D. | 4Z+14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气有毒,不可用于自来水的杀菌消毒 | |
| B. | Al(OH)3受热分解生成H2O并吸收大量的热量,可用作阻燃剂 | |
| C. | 二氧化硅不与强酸反应,可用玻璃容器盛放氢氟酸 | |
| D. | Na2O2具有强氧化性,可用作呼吸面具的供氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
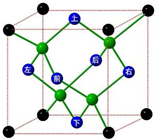 A、B、C、D、E、F六种元素的原子序数依次递增.已知:
A、B、C、D、E、F六种元素的原子序数依次递增.已知:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
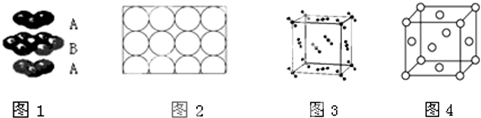
| A. | 钛和钾都采取图1的堆积方式 | |
| B. | 图2为金属原子在二维空间里的非密置层放置,此方式在三维空间里堆积,仅得简单立方堆积 | |
| C. | 图3是干冰晶体的晶胞,晶胞棱长为a cm,则在每个CO2周围最近且等距离的CO2有8个 | |
| D. | 图4是一种金属晶体的晶胞,它是金属原子在三维空间以密置层采取ABCABC…堆积的结果 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com