
铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式_________。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应_________________,负极反应_________________。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤:________________________________。
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
| 提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu |
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。
有关反应的化学方程式_____________、_______________。
劣质不锈钢腐蚀的实验现象:__________________________。
答案 (1)2Fe3++Cu===2Fe2++Cu2+
(2)装置图

正极反应:Fe3++e-===Fe2+(或2Fe3++2e-===2Fe2+)
负极反应:Cu===Cu2++2e-(或Cu-2e-===Cu2+)
(3)①通入足量氯气将Fe2+氧化成Fe3+;②加入CuO调节溶液的pH至3.2~4.7;③过滤
(4)CuO+H2SO4=CuSO4+H2O CuSO4+Fe=FeSO4+Cu 不锈钢表面有紫红色物质生成
解析 (2)根据氧化还原反应2Fe3++Cu===2Fe2++Cu2+设计原电池,负极发生氧化反应,Cu失电子作负极,正极选择比Cu活动性弱的金属或碳棒,电解质溶液为FeCl3溶液。
(3)根据表中的数据知如用直接沉淀法,Cu2+也被消耗。根据提供的试剂,将Fe2+氧化为Fe3+,再调节溶液的pH,为了不引入新的杂质离子,选择CuO而不选NaOH溶液。
(4)不锈钢的主要成分是Fe,由题中劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显,再根据提供的试剂可知首先要制备出盐溶液,选择硫酸和CuO制备出硫酸铜溶液,再根据Fe和硫酸铜发生置换反应设计出实验。


科目:高中化学 来源: 题型:
M元素的1个原子失去2个电子转移到Y元素的2个原子中去,形成离子化合物Z。下列说法中正确的是( )
A.Z可以表示为MY
B.Z可表示为M2Y
C.Z的电子式可表示为M2+[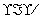
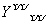 :]
:]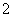
D.M形成+2价阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
有如下两个反应:
①2HCl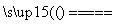 H2+Cl2 ②2HCl
H2+Cl2 ②2HCl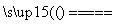 H2↑+Cl2↑
H2↑+Cl2↑
关于这两个反应的叙述中错误的是( )
A.①②两反应都是氧化还原反应
B.①②两反应中的能量转换方式都是热能转变为化学能
C.②反应是电能转变为化学能
D.①反应是热能转变为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
可再生能源是我国重要的能源资源,在满足能源需求、改变能源结构,减少环境污染、促进经济发展等方面具有重要作用。应用太阳能光伏发电技术,是实现节能减排的一项重要措施。
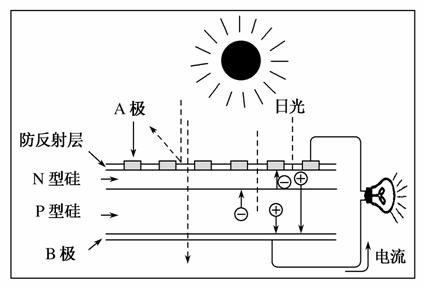
下列分析不正确的是( )
A.风能、太阳能、生物质能等属于可再生能源
B.推广可再生能源有利于经济可持续发展
C.上图是太阳能光伏电池原理图,图中A极为正极
D.光伏发电池能量转化方式是太阳能直接转变为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
物质分类的依据通常是根据它的组成和性质,下列仅从组成角度对物质分类的是( )
A.硫酸钠是钠盐、硫酸盐、正盐
B.二氧化硫是氧化物、酸酐、有漂白性的物质
C.氢氧化钠是一元碱、易溶性碱、强碱
D.碳酸氢钠是钠盐、酸式盐、易分解的盐
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学在烧水时,不小心把水洒在炉火上,结果发现炉火更旺了,原因是H2O和炽热的碳反应生成了水煤气(CO和H2),反应方程式为:C+H2O(g)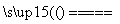 CO+H2,下列关于该反应说法正确的是( )
CO+H2,下列关于该反应说法正确的是( )
A.该反应中C失电子,被还原
B.该反应中H2得电子,被还原
C.该反应中,每转移2 mol e-则生成1 mol H2
D.该反应属于复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )
A.乙醇和乙酸都是常用调味品的主要成分
B.乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高
C.乙醇和乙酸都能发生氧化反应
D.乙醇与乙酸反应生成乙酸乙酯,说明乙醇具有碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是Zn和Cu形成的原电池,则下列结论中正确的是( )
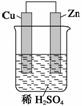 ①铜为阳极,锌为阴极;②铜极上有气泡;③SO向铜极移动;④若有0.5 mol电子流经导线,则可产生0.25 mol气体;⑤电子的流向是铜到锌;⑥正极反应式:Cu+2e-===Cu2+。
①铜为阳极,锌为阴极;②铜极上有气泡;③SO向铜极移动;④若有0.5 mol电子流经导线,则可产生0.25 mol气体;⑤电子的流向是铜到锌;⑥正极反应式:Cu+2e-===Cu2+。
A.①②③ B.②④
C.④⑤⑥ D.③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com