
 ,当有1mol Cl2生成时,氧化产物与还原产物的质量之比为
,当有1mol Cl2生成时,氧化产物与还原产物的质量之比为| 5 |
| 3 |
| 1 |
| 3 |
 .
.


科目:高中化学 来源: 题型:
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 1 | ||||||||
| 2 | A | |||||||
| 3 | B | C | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
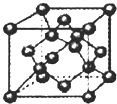 常见元素A、B、C、D,其原子结构的相关信息如下表:
常见元素A、B、C、D,其原子结构的相关信息如下表:| 元素 | 相关信息 |
| A | 核外电子总数等于该基态原子电子层数 |
| B | 最外层电子数是次外层电子数的2倍 |
| C | 基态原子L电子层中有3个未成对电子 |
| D | 生活中大量使用的合金制品,工业上可用电解其氧化物的方法制取其单质 |
| E | 外围电子排布为(n+1)d3n(n+2)sn |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 熔点(℃) | 密度(g/cm3) | 硬度(金刚石为10) | 导电性(银为100) | |
| 某铁合金 | 2500 | 3.00 | 7.4 | 2.3 |
| 铁 | 1535 | 7.86 | 4.5 | 17 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:
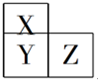 X、Y、Z、T、V为5种短周期元素,X、Y、Z在周期表中位置如图所示,这三种元素原子序数之和是41,X和T在不同条件下反应,可以生成化合物T2X(白色固体)和T2X2(淡黄色固体)两种化合物,V单质在Z单质中燃烧产生苍白色火焰,产物溶于水能使石蕊试液变红,则:
X、Y、Z、T、V为5种短周期元素,X、Y、Z在周期表中位置如图所示,这三种元素原子序数之和是41,X和T在不同条件下反应,可以生成化合物T2X(白色固体)和T2X2(淡黄色固体)两种化合物,V单质在Z单质中燃烧产生苍白色火焰,产物溶于水能使石蕊试液变红,则:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、难溶于水的电解质一定是弱电解质 |
| B、强电解质在水溶液中的电离过程是不可逆的 |
| C、易溶于水的电解质一定是强电解质 |
| D、强电解质的水溶液导电能力一定比弱电解质水溶液的导电能力强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在甲苯中加入少量酸性高锰酸钾溶液,振荡后褪色,正确的解释是由于侧链与苯环的相互影响,使侧链和苯环均易被氧化 |
| B、用核磁共振氢谱鉴别1-丙醇和2-丙醇 |
| C、间二溴苯仅有一种空间结构可证明苯分子中不存在单双键交替的结构 |
| D、甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com