
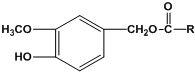
 (R为烃基)
(R为烃基)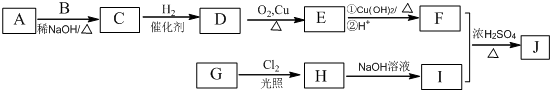
 .
. .
. (写结构简式).
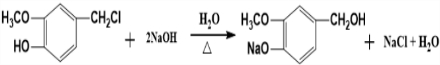
(写结构简式). 分析 D氧化得到E、E氧化得到F,则D中存在-CH2OH结构,E含有-CHO,F含有-COOH,F与I反应得到J,J的分子式为C15H22O4,结合J的结构特点,可知F为C6H13COOH.A、B和E为同系物,其中B的相对分子质量为44,则B为CH3CHO,A分子中碳原子数目为5,A的核磁共振氢谱显示有两组峰,则A为(CH3)3CCHO,A与B反应得到C,C与氢气反应得到D,则C为(CH3)3CCH=CHCHO,D为(CH3)3CCH2CH2CH2OH,E为(CH3)3CCH2CH2CHO,F为(CH3)3CCH2CH2COOH.G与氯气光照发生侧链烃基上取代反应生成H,H发生卤代烃水解反应得到I,则
可知I为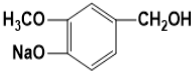 ,G为
,G为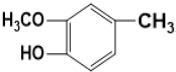 ,H为
,H为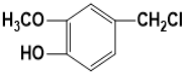 ,据此解答.
,据此解答.
解答 解:D氧化得到E、E氧化得到F,则D中存在-CH2OH结构,E含有-CHO,F含有-COOH,F与I反应得到J,J的分子式为C15H22O4,结合J的结构特点,可知F为C6H13COOH.A、B和E为同系物,其中B的相对分子质量为44,则B为CH3CHO,A分子中碳原子数目为5,A的核磁共振氢谱显示有两组峰,则A为(CH3)3CCHO,A与B反应得到C,C与氢气反应得到D,则C为(CH3)3CCH=CHCHO,D为(CH3)3CCH2CH2CH2OH,E为(CH3)3CCH2CH2CHO,F为(CH3)3CCH2CH2COOH.G与氯气光照发生侧链烃基上取代反应生成H,H发生卤代烃水解反应得到I,则
可知I为 ,G为
,G为 ,H为
,H为 .
.
(1)G为 ,所含官能团的名称为羟基、醚键,
,所含官能团的名称为羟基、醚键,
故答案为:羟基、醚键;
(2)由A和B生成C的化学方程式为:(CH3)3CCHO+CH3CHO$→_{△}^{稀NaOH}$(CH3)3CCH=CHCHO+H2O,
故答案为:(CH3)3CCHO+CH3CHO$→_{△}^{稀NaOH}$(CH3)3CCH=CHCHO+H2O;
(3)由C生成D的反应类型为加成反应,D为(CH3)3CCH2CH2CH2OH,名称为:4,4-二甲基-1-戊醇,
故答案为:加成反应;4,4-二甲基-1-戊醇;
(4)由H生成I的化学方程式为: ,
,
故答案为: ;
;
(5)J的结构简式为: ,
,
故答案为: ;
;
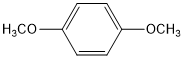
(6)G( )的同分异构体中,苯环上的一氯代物只有一种,可以含有2个-CH2OH且处于对位,或含有2个-OCH3且处于对位,可以含有4个取代基,为2个-OH、2个-CH3,当2个甲基相邻时,另外2个-OH分别与甲基相邻,或分别与甲基处于间位,当2个甲基处于间位时,另外2个-OH处于对位且分别与甲基相邻、相间,当2个甲基对位时,2个-OH分别与2个甲基相邻且2个羟基处于对位,或者2个羟基处于对位,或者2个-OH分别与1个甲基相邻,故符合条件的同分异构共有8种,核磁共振氢谱显示2组峰的是
)的同分异构体中,苯环上的一氯代物只有一种,可以含有2个-CH2OH且处于对位,或含有2个-OCH3且处于对位,可以含有4个取代基,为2个-OH、2个-CH3,当2个甲基相邻时,另外2个-OH分别与甲基相邻,或分别与甲基处于间位,当2个甲基处于间位时,另外2个-OH处于对位且分别与甲基相邻、相间,当2个甲基对位时,2个-OH分别与2个甲基相邻且2个羟基处于对位,或者2个羟基处于对位,或者2个-OH分别与1个甲基相邻,故符合条件的同分异构共有8种,核磁共振氢谱显示2组峰的是 ,
,
故答案为: .
.
点评 本题考查有机物推断与合成,充分利用反应条件、J的结构特点与分子式进行推断,需要学生熟练掌握官能团的性质与转化,侧重考查学生分析推理能力,难度中等.


科目:高中化学 来源: 题型:解答题
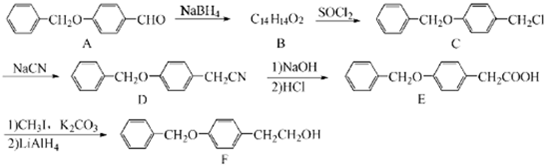
 ;由C→D的反应类型是:取代反应.
;由C→D的反应类型是:取代反应.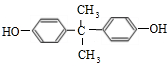
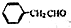 为原料制备
为原料制备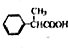 的合成路线示意图(无机试剂任用).合成路线示意图例如题干.
的合成路线示意图(无机试剂任用).合成路线示意图例如题干.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 将洁净的三种金属片X、Y和Z分别放置在浸有食盐溶液的滤纸上并压紧(如图).每次实验时,电压表指针的偏移方向和读数如下表.已知构成两电极的金属,活泼性相差越大,则电压越大.对X、Y、Z和铜四种金属的下列说法,不正确的是( )
将洁净的三种金属片X、Y和Z分别放置在浸有食盐溶液的滤纸上并压紧(如图).每次实验时,电压表指针的偏移方向和读数如下表.已知构成两电极的金属,活泼性相差越大,则电压越大.对X、Y、Z和铜四种金属的下列说法,不正确的是( )| 金属片 | 电子流向 | 电压(V) |
| X | X→Cu | +0.78 |
| Y | Cu→Y | -0.15 |
| Z | Z→Cu | +1.35 |
| A. | Z金属可作为牺牲阳极保护法的阳极,保护Y金属 | |
| B. | Y金属不能从硫酸溶液中置换出氢气 | |
| C. | 三种金属的活泼性顺序为:Y>X>Z | |
| D. | Z和Y能构成电压最大的原电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加热胆矾失去结晶水的过程称风化 | |
| B. | 在饱和溶液中,溶质溶解的速率等于结晶速率 | |
| C. | 原电池是把电能转化为化学能的装置 | |
| D. | 电能是二次能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某校化学实验兴趣小组为了探究实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),完成下列问题.
某校化学实验兴趣小组为了探究实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),完成下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢铁腐蚀的负极反应为:Fe-3e-=Fe3+ | |
| B. | Mg-Al及NaOH溶液构成的原电池中负极材料为Mg | |
| C. | 无隔膜电解饱和NaCl溶液所得产物之一是“84”消毒液中的有效成分NaClO | |
| D. | H2-O2燃料电池中电解液为H2SO4,则正极反应式为:O2+4e-=2O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中加水,$\frac{c(HC{O}_{3}^{-})•c(O{H}^{-})}{c(C{O}_{3}^{2-})}$增大 | |
| B. | 加入Na2CO3固体,$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$减小 | |
| C. | 升高温度,平衡常数减小 | |
| D. | 通入CO2,溶液pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
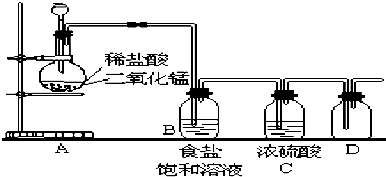
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17g NH3所含的电子数是 10NA | |
| B. | 常温常压下,22.4L氧气含氧原子数为2NA | |
| C. | 5.6g铁粉与足量Cl2反应,失去的电子数为0.2NA | |
| D. | 2.3g金属钠全部变成钠离子时失去的电子数是0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com