


科目:高中化学 来源:江西省九江一中2011-2012学年高一上学期期中考试化学试题 题型:058
实验室中有一瓶氯化钾和氯化钙的固体混和物,通过下面的实验除去氯化钾中氯化钙,并利用纯净的氯化钾配制一定浓度的氯化钾溶液.根据实验步骤填写下列空白.

回答下列问题
(1)加入的A是________.(填分子式,下同)
(2)操作②的名称是________.操作①、②均要用到的玻璃仪器有________.
(3)B物质是________,加入过量的B反应的离子方程式为________.
(4)称取一定量纯净的KCl,配制一定浓度的氯化钾溶液.
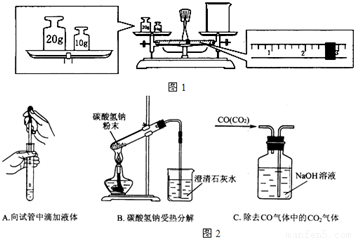
(ⅰ)某同学用托盘天来称取一定质量的KCl,称法如下图所示,天平的指针在标尺中间.此操作是否正确________(填正确或不正确);若按此操作称量,所称KCl的实际质量为________g (已知烧杯的质量为12.9克).

(ⅱ)某学生将准确称量的KCl固体放入烧杯中,加入约30毫升蒸馏水,用玻璃棒搅拌使其溶解.将溶液由烧杯倒入100毫升容量瓶中,然后往容量瓶中小心地加蒸馏水,直到液面接近刻度1-2厘米处,改用胶头滴管加蒸馏水,使溶液凹面最低点恰好与刻度相切,把容量瓶盖紧,再振荡摇匀.该生操作中的错误是________和________.
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(共13分)〔一〕实验室用氢氧化钠配制1.00mol/L的氢氧化钠溶液0.2L,回答下列问题
(1)下列有关使用托盘天平的叙述,正确的是 。
A.称量前先调节天平的零点。
B.称量时左盘放被称量物,右盘放砝码。
C.氢氧化钠必须放在玻璃器皿里称量。
D.称量时,应先加质量小后加质量大的砝码至天平平衡。
E.称量完毕,应把天平放回砝码盒中。
(2)某同学用托盘天平称取一盛有氢氧化钠药品的烧杯,若左盘上放有30g砝码,游码位置如下图所示,天平的指针指在标尺的中间。则烧杯和粉剂的总质量为_________克。
〔二〕用98%的浓H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的稀H2SO4 500ml的操作步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④转移、洗涤 ⑤定容、摇匀 ,请按要求填空:
(1)如果实验室有15mL、20mL、50mL量筒,应选用 mL量筒最好。
(2)第⑤步实验的操作是(文字叙述)_______________________________________________
(3)某学生的下列操作中使浓度偏低的原因是: 。
① 用量筒量取浓硫酸时,俯视读数。
② 量筒中浓硫酸全部转入烧杯中稀释后,再转移到100ml容量瓶中,烧杯未洗涤。
③ 用玻璃棒引流,将溶液转移到容量瓶中有溶液流到了容量瓶外面。
④ 浓硫酸在小烧杯中稀释后,没有冷却就马上转移入容量瓶。
⑤ 用胶头滴管加蒸馏水时,加入过快而使液面超过了刻度线,立即用滴管吸去多余的水,使溶液凹石刚好与刻度线相切。
⑥ 滴加入蒸馏水,使溶液凹面刚好与刻度线相切,盖上瓶塞反复摇匀后,静置,发现液石比刻度线低,再加水至刻度线。
查看答案和解析>>
科目:高中化学 来源: 题型:

回答下列问题:
(1)实验开始时,欲使装置中的稀硫酸和黄铜中的锌发生反应,应进行的操作是____________
______________________;反应结束后,恢复至反应前的温度,对碱式滴定管进行准确读数前,应进行的必要操作是:______________________________________________________
(2)为了保证实验结果的准确,请你将本实验过程中需直接测定的有关物理量填入下表中(用文字说明,不必填满):
① | ② | ③ | ④ | ⑤ | ⑥ |
|
|
|
|
|
|
(3)某同学还想利用托盘天平和下图所示装置完成锌的质量分数和锌的相对原子质量的测定实验。

①该实验过程中,必须对反应后所剩的固体进行洗涤、干燥,如何确定所得固体是干燥的_____________________________________________________________________。
②请你从该实验装置、中学化学实验室的现有条件两方面,对该实验方案的可行性进行评价:___________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com