
| ���巢��װ�� | 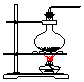 a | 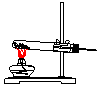 b |  c |
| �����ռ�װ�� | 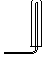 2 | 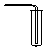 �� | 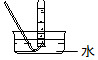 �� |
���� ��1�����ݷ�Ӧԭ��2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��Ӧ��״̬�ͷ�Ӧ����ѡ����װ�ã������ܶ�С�ڿ����ܶȣ�������ˮ��Ӧ���������ſ������ռ���
��2�����ݰ�����������ˮ��1���ˮ�ܽ�700�����������ϰ�����ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ���������笠����������������ӽ��
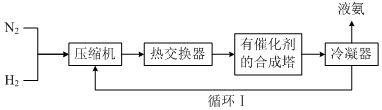
��3��N2��H2�ڸ��¸�ѹ�������·�Ӧ����NH3����ͼ��֪�������п�ѭ�����õ����ʣ�
��4���� CO2ͨ�뵽�����ı���ʳ��ˮ�У�NaCl��CO2��NH3��H2O��Ӧ����NaHCO3�������Ȼ�泥�N��P��Asԭ�Ӱ뾶��������ʹ��N-H��P-H��As-H�����������������ȶ���������
��5����NH4��2SO4��ҺΪǿ�������Σ�����笠�ˮ��ʹ��Һ�����ԣ���Һ�д��ڵ���غ�������غ㣬����غ�Ϊ��[NH4+]+[H+]=2[SO42-]+[OH-]�������غ�Ϊ��2[SO42-]=[NH4+]+[NH3•H2O]��
��� �⣺��1�����ݷ�Ӧԭ��2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O����֪�Ʊ�������Ӧ��״̬Ϊ��������壬��Ӧ����Ϊ���ȣ�����Ӧѡ��װ��b�Ʊ���
�����ܶ�С�ڿ����ܶȣ�������ˮ��Ӧ���������ſ������ռ�������Ӧѡ��װ�â��ռ���
�ʴ�Ϊ��b���٣�
��2��������������ˮ��1���ˮ�ܽ�700���������������100mLע�����ռ���50mL�����İ�����Ȼ���ٳ�ȡ10mL���з�̪��Һ������ˮ��������Ƥ�������ͷ�������ע������������ʣ�࣬������ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ���������笠�����������������ʹ��Һ�Լ��ԣ����ӷ���ʽΪ��NH3+H2O?NH3•H2O?NH4++OH-������������̪���ɫ��
�ʴ�Ϊ���ޣ��죻NH3+H2O?NH3•H2O?NH4++OH-��
��3��N2��H2�ڸ��¸�ѹ�������·�Ӧ����NH3����ͼ��֪�������п�ѭ�����õ����ʣ��ʴ�Ϊ��d��
��4���� CO2ͨ�뵽�����ı���ʳ��ˮ�У�NaCl��CO2��NH3��H2O��Ӧ����NaHCO3�������Ȼ�泥���Ӧ��ѧ����ʽΪ��NaCl+CO2+NH3+H2O=NaHCO3��+NH4Cl��N��P��Asԭ�Ӱ뾶��������ʹ��N-H��P-H��As-H�����������������ȶ�������������NH3��PH3��AsH3�����⻯�����ȶ�����ǿ������˳����NH3��PH3��AsH3���ʴ�Ϊ��NaCl+CO2+NH3+H2O=NaHCO3��+NH4Cl��NH3��PH3��AsH3��N��P��Asԭ�Ӱ뾶��������ʹ��N-H��P-H��As-H�����������������ȶ���������
��5����NH4��2SO4��ҺΪǿ�������Σ�����笠�ˮ��ʹ��Һ�����ԣ�ˮ�ⷽ��ʽΪ��NH4++H2O=NH3•H2O+H+����Һ�д��ڵ���غ�������غ㣬����غ�Ϊ��[NH4+]+[H+]=2[SO42-]+[OH-]�������غ�Ϊ��2[SO42-]=[NH4+]+[NH3•H2O]
�ʴ�Ϊ���NH4++H2O=NH3•H2O+H+������غ�Ϊ��[NH4+]+[H+]=2[SO42-]+[OH-]���������غ�Ϊ��2[SO42-]=[NH4+]+[NH3•H2O]��
���� ���⿼���˰�����ʵ�����Ʊ��������ϳ�����;�Լ�����ˮ��ԭ������Ϥ����ʵ�����Ʊ�ԭ������Ϥ�����������ǽ���ؼ�����Ŀ�ѶȲ���


 ���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д�
���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д� ���Ͱ�ͨ������ϵ�д�
���Ͱ�ͨ������ϵ�д� �ٷ�ѧ����ҵ��������ϵ�д�
�ٷ�ѧ����ҵ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �������й�˵����ȷ���ǣ�������
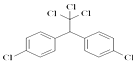
�������й�˵����ȷ���ǣ�������| A�� | �������� | |
| B�� | DDT��ȫȼ�պ�ֻ����CO2��H2O�������� | |
| C�� | ����������̼ | |
| D�� | �˴Ź�����������ʾ��2��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Լ�ƿ��ȡ�����κ�ҩƷ������ʣ����ٷŻ�ԭ�Լ�ƿ | |
| B�� | ���ǡ��ƾ���ˮ��Һ������״̬�¾������磬�������Ǿ��Ƿǵ���� | |
| C�� | ��������ȶ�����������Ȼ���п���������̬���� | |
| D�� | ��Ӿ�����֤���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2O2��Cu��ϡ����ķ�Ӧ������� | |
| B�� | ��Ӧ�����еĻ�ԭ������SO2 | |
| C�� | ��Cu������ǡ����ȫ��Ӧ����ԭϡ��������ʵ���Ũ��Ϊ0.75mol•L-1 | |
| D�� | ��Ӧ�����У���ԭ���������������ʵ���֮��Ϊ1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3��5 | B�� | 1��2 | C�� | 8��11 | D�� | 18��8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������CuSO4•5H2O���ǻ���� | |
| B�� | ���ȵ���ʧȥ�ᾧˮ�Ĺ����Ƿ绯 | |
| C�� | �Ȼ�������ˮ���������⣬���Կ�������� | |
| D�� | �ӱ�����Һ�������ľ��嶼���нᾧˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol H2SO4�� 1 mol Ba��OH��2��ȫ��Ӧ�ų������������к��� | |
| B�� | �������ϡ��Һ���к��Ȳⶨʵ�飬����кͷ�Ӧ��Ӧ��ƫ�� | |
| C�� | һ����H2ȼ��������̬ˮʱ������Һ̬ˮʱ�ų��������� | |
| D�� | ��101 kPaʱ��1 molH2��Cl2��ȼ��ʱ�ų�������Ҳ��H2��ȼ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com