
【题目】下列选项中涉及的离子方程式书写正确的是( )
A. 向Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2OH-+2HCO![]() = CaCO3↓+CO
= CaCO3↓+CO![]() +2H2O
+2H2O
B. 室温下测得NH4HSO4溶液的pH<7,主要是因为存在:NH4++H2O![]() NH3·H2O+H3O+
NH3·H2O+H3O+
C. 用重铬酸钾溶液滴定草酸:Cr2O![]() +14H++3C2O
+14H++3C2O![]() -=2Cr3++6CO2↑+7H2O
-=2Cr3++6CO2↑+7H2O
D. 向AgCl沉淀中加入过量的氨水使AgCl溶解:AgCl+2NH3·H2O = [Ag(NH3)2]++Cl-+2H2O
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】利用光伏电池与膜电解法制备Ce(SO4)2溶液的装置如下图所示,下列说法不正确的是

A. 该离子交换膜为阴离子交换膜,SO42-由右池向左池迁移
B. 电解池中发生的总反应为Cu2++2Ce3+=Cu+2Ce4+
C. 该装置工作时的能量转化形式只有两种
D. 由P电极向N电极转移0.1mol电子时,阳极室生成33.2gCe(SO4)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列试剂保存方式不正确的是
A. 钠保存于水中 B. 浓硝酸保存在玻璃瓶中
C. HF溶液保存于塑料瓶中 D. 稀NaOH溶液保存于带胶塞的玻璃瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:

下列有关叙述正确的是
A.可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
B.贝诺酯分子中有三种含氧官能团
C.乙酰水杨酸和对乙酰氨基酚均能与Na2CO3 溶液反应
D.贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分。当左边充入1molN2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置(左、右两侧温度相同)。右侧CO2与CO分子数之比为

A. 1:3 B. 3:1 C. 1:2 D. 2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿原酸被誉为“第七类营养素”,具有广泛的杀菌、消炎功能,其结构简式如右下图所示。下列有关绿原酸的说法中正确的是( )

①绿原酸分子中含有3种官能团
②1 mol绿原酸最多能与7molNaOH发生反应
③绿原酸能发生取代反应、加成反应和消去反应
④绿原酸能使酸性高锰酸钾溶液、浓溴水褪色,但反应原理不同
A. ①③ B. ②③ C. ①④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的离子,能在溶液中大量共存的是( )
A.Ba2+、OH﹣、NO3﹣、Na+
B.NH4+、OH﹣、SO42﹣、K+
C.Ca2+、H+、Cl﹣、CO32﹣
D.Cu2+、SO42﹣、Ba2+、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能较好说明乙醇分子结构简式为C2H5OH,而不是CH3OCH3的事实是( )
A. 1mol乙醇完全燃烧只生成2molCO2和3molH2O
B. 乙醇无同分异构体
C. 0.1mol乙醇与足量钠反应只产生0.05mol氢气
D. 乙醇与水以任意比例互溶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置中,设计合理的是
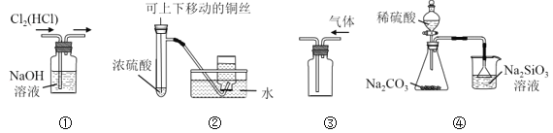
A. 图①用于除去Cl2中混有的HCl气体
B. 图②用于制取并收集少量SO2气体
C. 图③用于排空气法收集CO2气体
D. 图④比较硫、碳、硅三种元素的非金属性强弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com