
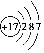 ��
������ ��1����ԭ�ӵĺ�����17�����ӣ�������17�����ӣ�
��2��̼�������׳�С�մ�
��3��ʵ�����ö������̺�Ũ���������ȡ������
��4��ľ̿�ڼ��������±�Ũ��������Ϊ������̼��Ũ���ᱻ��ԭΪ�������ݴ˷�����
��� �⣺��1����ԭ�ӵĺ�����17�����ӣ���17������ɣ�������17�����ӣ���ԭ�ӽṹʾ��ͼΪ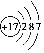 ���ʴ�Ϊ��
���ʴ�Ϊ��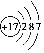 ��
��
��2��̼�������׳�С�մ�ѧʽΪNaHCO3���ʴ�Ϊ��NaHCO3��
��3��ʵ�����ö������̺�Ũ���������ȡ�������������̽�Ũ��������Ϊ�������������̱���ԭΪ�Ȼ��̣�ͬʱ��ˮ���ɣ��ʻ�ѧ����ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;����\;}}{\;}$MnCl2+Cl2��+2H2O�����ӷ���ʽΪMnO2+2Cl-+4H+$\frac{\underline{\;����\;}}{\;}$Mn2++Cl2��+2H2O���ʴ�Ϊ��MnO2+2Cl-+4H+$\frac{\underline{\;����\;}}{\;}$Mn2++Cl2��+2H2O��
��4��ľ̿�ڼ��������±�Ũ��������Ϊ������̼��Ũ���ᱻ��ԭΪ����������ˮ���ɣ��ʻ�ѧ����ʽΪC+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+2SO2��+2H2O���ʴ�Ϊ��C+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+2SO2��+2H2O��
���� ���⿼���˻�ѧ����ʽ�����ӷ���ʽ�Լ����ʵ��׳ƺͻ�ѧʽ����д�����ݣ��ѶȲ������ڻ�����֪ʶ�Ŀ��飮


 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д� ��Ȥ����¹�֪��ϵ�д�
��Ȥ����¹�֪��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬϵ������ʽ��ͬ��ͬ���칹��ķ���ʽ��ͬ | |
| B�� | ͨʽ��ͬ����ͬϵ���Է���������ͬ����ͬ���칹�� | |
| C�� | ͬϵ���ͨʽ��ͬ��ͬ���칹�����Է���������ͬ | |
| D�� | ��������ͬ����ͬϵ���̼����ͬ����ͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2 mol•L-1 ��Na2SO4��Һ�к���4 NA��Na+ | |
| B�� | ������0.1 mol FeCl3�ı�����Һ��ε���������ˮ�У��õ�Fe��OH��3������ĿΪ0.1 NA | |
| C�� | �ڱ�״���£�11.2 L�����к���NA����ԭ��1100�� | |
| D�� | 7.8 g Na2O2����������ĿΪ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ�������ԣ�Co2O3��Cl2 | |
| B�� | �μӷ�Ӧ��HClȫ����Co2O3���� | |
| C�� | ÿ����1Ħ������������1Ħ��Co2O3 | |
| D�� | �Ʊ���ͬ��������������Co2O3������MnO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ȼ���в���������̬���� | |
| B�� | ���ڿ����е�ȼ�ղ����Ƕ��������ڴ����е�ȼ�ղ������������� | |
| C�� | ����������ʹ���з�̪������������Һ��ɫ����������Ư���� | |
| D�� | Ũ�������������SO2��CO��Cl2������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ�Ľṹ��ʽ��CH2CH2 | B�� | ȩ���ĵ���ʽ��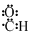 | ||
| C�� | ��������ʽ��CH2O | D�� | �Ҵ����ӱ���ģ�ͣ�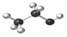 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
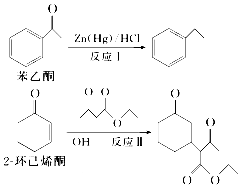 ��Ӧ��ͷ�Ӧ�����л��ϳ��е���Ҫ��Ӧ�������й�˵����ȷ���ǣ�������
��Ӧ��ͷ�Ӧ�����л��ϳ��е���Ҫ��Ӧ�������й�˵����ȷ���ǣ�������| A�� | ����ͪ��һ�ȴ�����6��ͬ���칹�� | |
| B�� | ����ͪ����Ӧ�����ò��������ԭ�Ӳ�������ͬһƽ���� | |
| C�� | ��Ӧ��Ϊȡ����Ӧ | |
| D�� | ��Ӧ�������ǿ���������½��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com