
某研究性学习小组的同学通过对亚硫酸钠组成元素的价态进行分析后认为Na2SO3溶液在存放过程中有可能变质,若已变质,则相应反应的化学方程式为__________________________。
(1)甲同学设计了如下两种方案来检验Na2SO3溶液是否变质。
方案Ⅰ:取样,加入稀盐酸有气泡生成,认为Na2SO3溶液没有变质。
方案Ⅱ:取样,加入氯化钡溶液有白色沉淀生成,认为Na2SO3溶液完全变质。
乙同学认为上述两种方案均不合理,乙同学作出判断的依据分别是方案Ⅰ:________;方案Ⅱ:________。
(2)乙同学设计如图所示装置(夹持装置已略去)探究Na2SO3溶液是否变质,量取60 mL标签上注明为1.0 mol·L-1的Na2SO3溶液放入A装置中,通过测量生成的SO2质量的方法来判断其是否变质。
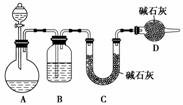
①D装置的作用是________,该实验装置中还存在一个明显的缺陷是________________,分液漏斗中应加入足量的________(填字母);
a.浓硝酸 b.65%硫酸
c.浓盐酸 d.20%硫酸
②改进缺陷后再进行实验,若实验前后测得C装置增重3.2 g,则Na2SO3变质的百分率是__________。
(3)丙同学认为若只是确定Na2SO3是否变质,乙的方案太复杂了,他认为只需要试管、胶头滴管、盐酸及氯化钡溶液就可以达到目的(不考虑对环境的影响),请你发表自己的看法(若不同意,请说明理由;若同意,请写出主要操作、现象及结论):______________________。
答案 2Na2SO3+O2===2Na2SO4
(1)Na2SO3溶液部分变质时滴加稀盐酸也会产生气泡
BaSO3也难溶于水,故Na2SO3未变质或部分变质时也会产生白色沉淀
(2)①防止空气中的水蒸气及酸性气体进入C装置中 缺少一个驱赶残留SO2的操作步骤(或其他合理答案) b ②16.7%
(3)同意丙的看法。具体操作为取适量Na2SO3样品溶液于试管中,加入足量BaCl2溶液后,再加入足量稀盐酸,若生成的白色沉淀全部溶解,则Na2SO3没有变质;若部分溶解,则Na2SO3部分变质;若完全不溶解,则Na2SO3全部变质
解析 亚硫酸盐变质是由于其具有较强的还原性,能被空气中的氧气氧化成硫酸盐。(1)当Na2SO3溶液部分变质时,加入稀盐酸也会产生SO2;由于BaSO3和BaSO4均难溶于水,无论Na2SO3溶液是否变质,加入BaCl2溶液后均可形成白色沉淀,故两种方案均不合理。(2)①本实验是通过测量C装置在实验前后质量的变化来确定生成SO2的质量,故D装置的作用是防止空气中的水蒸气及酸性气体进入C装置中;因生成的SO2会有一部分留在A、B装置的上方,故应该有一个驱赶残留SO2气体的操作步骤;由于SO2在水中溶解度较大,故应使用浓度较大的酸,因浓硝酸能氧化SO2,浓盐酸具有较强的挥发性,故应选用65%硫酸;②若Na2SO3未变质,则所取溶液中Na2SO3的物质的量为0.06 mol,C装置增加的质量就是SO2的质量,其物质的量为0.05 mol,由此可知还有0.05 mol Na2SO3没有被氧化,则Na2SO3变质的百分率为(0.06 mol-0.05 mol)÷0.06 mol×100%≈16.7%。(3)丙同学的观点是正确的,因为只要检验出Na2SO3溶液中是否含有SO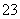 、SO
、SO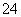 ,就可以确定其是否被氧化及是否全部被氧化。
,就可以确定其是否被氧化及是否全部被氧化。


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案科目:高中化学 来源: 题型:
x、y为两种元素的原子,x的阴离子与y的阳离子具有相同的电子层结构,由此可知
A.x的原子半径大于y的原子半径 B.x的电负性大于y的电负性
C.x的能层数性等于y的能层数 D.x的第一电离能小于y的第一电离能
查看答案和解析>>
科目:高中化学 来源: 题型:
有①Na2CO3溶液 ②CH3COONa溶液 ③NaOH溶液各25 mL,物质的量浓度均为0.1 mol/L,下列说法正确的是( )
A.3种溶液pH的大小顺序是③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是②
C.若分别加入25 mL 0.1 mol·L-1的盐酸后,pH最大的是①
D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>②
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用下列仪器,以乙醇、浓硫酸和溴为原料制备1,2二溴乙烷。已知1,2二溴乙烷熔点为9 ℃,C2H5OH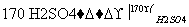 CH2===CH2↑+H2O。
CH2===CH2↑+H2O。
2C2H5OH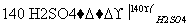 C2H5—O—C2H5+H2O
C2H5—O—C2H5+H2O
(乙醚)
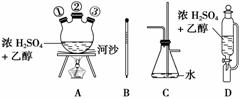

(1)如果气体流向为从左到右,正确的连接顺序是(短接口或橡皮管均已略去):B经A①插入A中,D接A②;A③接________接________接________接________。
(2)装置A中反应器的名称为________,仪器D的名称为________,河沙的作用为________。
(3)写出仪器C的两个作用:________________________________________________。
(4)温度计水银球的正确位置是_________________________________________________。
(5)反应管E中加入少量水及把反应管E置于盛有冷水的小烧杯中是因为________________________________________________________________________。
(6)若产物中有少量未反应的Br2,最好用________(填正确选项前的字母)洗涤除去。
a.饱和亚硫酸氢钠溶液
b.氢氧化钠溶液
c.碘化钠溶液
d.乙醇
(7)产品中可能会有的有机杂质是______,可用________方法除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的氧化铝膜。某研究性学习小组对铝表面氧化膜的保护作用展开了研究,他们查阅有关资料得知:尽管铝表面致密的氧化膜能使铝与其周围的介质(如空气、水等)隔绝,对铝制品起到保护作用,但铝制容器仍不能长期盛放或腌制咸菜。该小组同学设计了一个实验以探究其中的原因。他们的实验过程如下所示:
| 实验 | ||
| 编号 | 实验过程 | 实验现象 |
| 1 | 取一小片铝片于试管中,加入2 mL 1.0 mol·L-1盐酸 | 30 s时开始有少量气泡,然后产生气泡的速率逐渐加快,最后铝片消失 |
| 2 | 取一小片铝片于试管中,加入2 mL 0.5 mol·L-1硫酸 | 55 s时开始有少量气泡,然后产生气泡的速率逐渐加快,最后铝片消失 |
| 3 | 取一小片铝片于试管中,加入氯化铜稀溶液 | 3 min左右表面产生少量气泡,且铝表面析出一些红色固体 |
| 4 | 取一小片铝片于试管中,加入硫酸铜稀溶液 | 一直没有明显的变化 |
(1)你认为实验1、2中盐酸和硫酸的浓度分别为1.0 mol·L-1、0.5 mol·L-1的原因是__________________________________。
(2)根据该实验现象,你认为铝制容器不能长期盛放或腌制咸菜的原因是__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学反应速率的说法正确的是( )
A.化学反应速率是指一定时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加
B.化学反应速率为0.8 mol·L-1·s-1是1 s时某物质的浓度为0.8 mol·L-1
C.根据化学反应速率的大小可以知道化学反应进行的快慢
D.对于任何化学反应来说,反应速率越大,反应现象就越明显
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。已知高铁酸盐热稳定性差,工业上用湿法制备高铁酸钾的基本流程如下图所示:
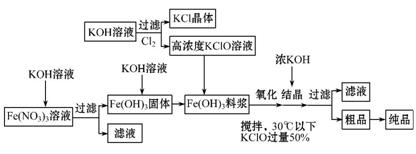
(1)上述氧化过程中,发生反应的离子方程式是 ,
控制反应温度30℃以下的原因是 。
(2)结晶过程中加入浓KOH溶液的作用是 。
(3)已知常温下Ksp[Fe(OH)3]=1.25×10-36,则Fe(NO3)3溶液中加入KOH溶液到
pH= 时,Fe3+才能完全沉淀(当溶液中某种离子浓度小于10-5mol·L-1时可看作完全沉淀,lg2=0.3,lg5=0.7),常温下反应Fe3++3H2O Fe(OH)3+3H+的平衡常数K= [水解生成的Fe(OH)3为胶体,其浓度不代入计算式,写出计算结果]。
Fe(OH)3+3H+的平衡常数K= [水解生成的Fe(OH)3为胶体,其浓度不代入计算式,写出计算结果]。
(4)最近,工业上用表面附有铁的氧化物的铁丝网作阳极,电解KOH溶液制备K2FeO4,优点是原料价廉,效率高。若用一表面附有Fe3O4的铁丝网20.0 g作阳极电解,当电路中通过1.4 mol电子时,铁丝网恰好电解完全。此时生成K2FeO4的质量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
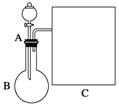 氨水是一种常用的化学试剂。
氨水是一种常用的化学试剂。
(1)以浓氨水和生石灰为原料,用如右装置为发生装置,可制取少量氨气。已知:NH3·H2O(浓)+CaO===Ca(OH)2+NH3↑。
①生石灰应该装在________(填“A”或“B”)中。
②试从电离平衡角度分析该实验中氨气逸出的原因:_______________。
③现要用试管和必要实验用品收集一试管氨气,请在C处补充相应收集装置。
(2)化学兴趣小组用氨水与硝酸银溶液配制好银氨溶液后,进行乙醛的银镜反应实验,但部分同学实验时间长,且效果不明显。影响乙醛银镜反应速率的因素有哪些呢?请你完成如下猜想:
①猜想:因素一:银氨溶液的pH大小;
因素二:________________。
②请你设计实验验证上述影响因素一,完成下表中内容。
提供试剂:乙醛、2%稀氨水、0.25 mol·L-1 NaOH溶液、盐酸、2% AgNO3溶液
实验用品:烧杯(装有热水)、试管
| 实验 步骤 | 实验操作 | 预期现象 及结论(步骤 1只填现象) |
| 1 | 在A、B两支洁净的试管中各加入1 mL 2%的AgNO3溶液,然后边振荡试管边逐滴滴入2%稀氨水,至最初产生的沉淀恰好完全溶解,此时制得pH均约为8的银氨溶液 | |
| 2 |
(3)取20.00 mL上述氨水于锥形瓶,滴加3滴甲基橙指示剂,用0.005 0 mol·L-1 的标准硫酸溶液滴定,滴定至锥形瓶溶液出现红色为终点,重复3次实验,平均消耗标准硫酸20.04 mL,则上述氨水的物质的量浓度为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com