
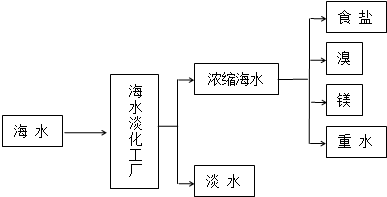
���� ��1��Ŀǰ������ˮ�ķ����ж��֣����÷��������������Լ����ӽ������ȣ��Դ˽��
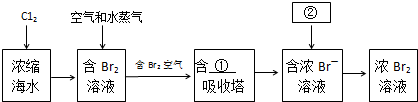
��2����Ũ����ˮ����ȡ�壬�Ƚ��������ӵ������õ��嵥�ʣ����ö������������嵥�ʸ����õ������ӣ�����ٴ�������������
��3��MgO���۵�Ϊ2852�桢�۵�ߣ����ʱ���ܸߣ�
��4��ʳ��ˮ�к�����������Mg2+��Ca2+��һ�����������ɳ��������ӽ���Ĥ�����ݵ��ʳ��ˮ�IJ���֮���ܷ�Ӧ��
��5���������η�����������ƽ��ʱH2��SiHCl3���ʵ���Ũ�ȣ��������ʼ���ʵ������ٸ���2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2NaOH��������������Ĵ�NaCl��������
��� �⣺��1��Ŀǰ������ˮ�ķ����ж��֣���ˮ��������ͨ�����õ��Ʊ���ˮ�ķ����У���������������
�ʴ�Ϊ����������������
��2����Ũ����ˮ����ȡ�壬�Ƚ��������ӵ������õ� �嵥�ʣ����ö������������嵥�ʵĸ����õ������ӣ�����ٴ��������������������з����Ļ�ѧ��Ӧ����ʽΪ��SO2+Cl2+2H2O=H2SO4+2HCl��
�ʴ�Ϊ��SO2��Cl2��SO2+Cl2+2H2O=H2SO4+2HCl��
��3��MgO���۵�Ϊ2852�桢�۵�ߣ����ʱ���ܸߣ����Թ�ҵ�ϣ��������MgCl2ұ������þ��
�ʴ�Ϊ��MgO�۵�ܸߣ������Ĵ������ܣ�
��4�����Լ����������ˮ�л���������Mg2+��Ca2+�����������»����ɳ����������ӽ���Ĥ������Ҫ�������ӽ�������ȥMg2+��Ca2+�����ʳ��ˮ�IJ������������������������ƣ����������������ܷ�Ӧ������������Ҳ�ܷ�Ӧ�����Ե��ʳ��ˮ�����ӽ���Ĥ�����н��У�
�ʴ�Ϊ�����Լ����������ˮ�л���������Mg2+��Ca2+�����������»����ɳ����������ӽ���Ĥ����ֹH2��C12��Ϸ�����ը��ͬʱ��ֹC1-���������ң��������Ի�ô�����NaOH��
��5����Ӧ����ʽ��֪��3SiCl4��g��+2H2��g��+Si��s��?4SiHCl3��g��
��ʼ����mol�� n 0
�仯����mol�� 2x x 4x
ƽ������mol�� n-2x 4x
��4x=0.020mol/L��20L=0.4mol��x=0.1mol��
n-2x=0.140mol/L��20L=2.8mol��n=3.0mol��
��2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2NaOH��
2mol 1mol
$\frac{2��58.5g}{1mol}$=$\frac{m��NaCl��}{3mol}$��
��ã�m��NaCl��=350g=0.35kg��
�ʴ�Ϊ��0.35��
���� ���⿼���˺�ˮ��Դ���ۺ����ã���Ŀ�Ѷ��еȣ���һ���ۺ������⣬�漰֪ʶ��Ƚ϶࣬��ֿ�����ѧ�����Ӧ�û���֪ʶ��������Ҫ��ѧ����������֪ʶ�ṹ�ͷ��������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
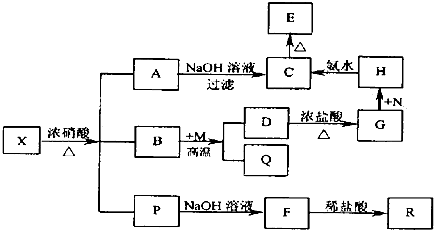
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ﵽƽ��������Ӧ��ֹͣ������Ӧ���ʵ����淴Ӧ������Ϊ0 | |
| B�� | ���տ�����0.2 mol NH3 | |
| C�� | ���{�¶ȣ���Ӧ�������� | |
| D�� | ��V����N2����V ����H2��=1��3ʱ��һ���ﻯѧƽ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Һ��ϡ���ᷴӦ��Ba2++SO42-+H++OH-=BaSO4��+H2O | |
| B�� | ���۵⻯����Һ�ڿ����б�����4I-+O2+2H2O=4OH-+2I2 | |
| C�� | �����������������Fe2O3+6H+=2Fe3++3H2O | |
| D�� | �ð�ˮ����������SO2���壺OH-+SO2=HSO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
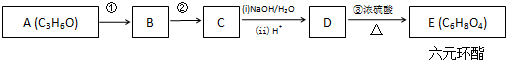
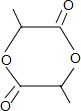 +2H2O��
+2H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NA �������������3mol �� �� | |
| B�� | 18gˮ�к���NA �Թµ��Ӷ� | |
| C�� | NA �����������к���2mol �м� | |
| D�� | NA ��������̼�����к���2mol �м� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
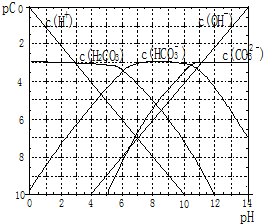 pC����pH����ָ��ϡ��Һ���������ʵ���Ũ�ȵij��ö�����ֵ����ij��Һ���ʵ�Ũ��Ϊ��1��10-3mol/L�������Һ�и����ʵ�pC=-lg1��10-3=3����֪H2CO3��Һ�д��ڵĻ�ѧƽ��Ϊ��CO2+H2O?H2CO3?H++HCO3-?2H++CO32-����ͼΪH2CO3��Һ��pC-pHͼ����ش��������⣺
pC����pH����ָ��ϡ��Һ���������ʵ���Ũ�ȵij��ö�����ֵ����ij��Һ���ʵ�Ũ��Ϊ��1��10-3mol/L�������Һ�и����ʵ�pC=-lg1��10-3=3����֪H2CO3��Һ�д��ڵĻ�ѧƽ��Ϊ��CO2+H2O?H2CO3?H++HCO3-?2H++CO32-����ͼΪH2CO3��Һ��pC-pHͼ����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������OH- | B�� | ������������ | ||
| C�� | ʯī���Ϸų����� | D�� | ʯī���Ϸų����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ���ֶ�����Ԫ��X��Y��Z��W��Ԫ�����ڱ��е����λ����ͼ��ʾ������Y�ǵ����Ϻ�����ߵĽ���Ԫ�أ������ж���ȷ���ǣ�������
���ֶ�����Ԫ��X��Y��Z��W��Ԫ�����ڱ��е����λ����ͼ��ʾ������Y�ǵ����Ϻ�����ߵĽ���Ԫ�أ������ж���ȷ���ǣ�������| A�� | 1molW�ĵ���������������ȼ��ת�Ƶ�������6NA | |
| B�� | ��YԪ�ص�����Һ���������ԣ�Ҳ�����Լ��� | |
| C�� | ZԪ�صĵ��ʺ������ﲻ�����κ��ᷢ����Ӧ | |
| D�� | X��H��OԪ���γɵĻ�����һ���ǹ��ۻ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com