
海洋约占地球表面的71%,具有十分巨大的开发潜力,目前的南海争端威胁到我们国家的核心利益。通过海水资源的开发利用不能得到的是
A.重水 B.淡水
C.石油、天然气 D.钠、钾、镁、溴
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年福建省高二下学期期末化学试卷(解析版) 题型:填空题
2015年8月12日,天津滨海新区爆炸事故确认有氰化钠(NaCN)、亚硝酸钠等,氰化钠毒性很强,遇水、酸会产生有毒易燃氰化氢气体。氰化氢的沸点只有26摄氏度,因此相当容易挥发进入空气,这就大大增加了中毒的风险。同时氰化钠遇到亚硝酸钠会发生爆炸。回答下列问题
(1)写出氰化钠遇水产生氰化氢的离子方程式 。
(2)爆炸现场约700吨的氰化钠大约需要900吨的双氧水来处理。氰化钠与双氧水相遇后,会释放出氨气同时析出白色晶体,使得氰化钠的毒性大大降低,写出氰化钠与双氧水反应的化学方程式 。
(3)氰化钠遇到亚硝酸钠能生成两种气体发生爆炸,写出化学反应方程式 。
(4)爆炸残留在废水中的CN- 可以用Cr2O72-处理,拟定下列流程进行废水处理,
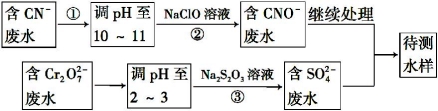
1)上述处理废水流程中主要使用的方法是 ;
A.混凝法 B.中和法 C.沉淀法 D.氧化还原法
2)②中反应后无气体放出,该反应的离子方程式为_______________________;
3)步骤③中,每处理0.4 mol Cr2O72 - 时转移电子2.4 mol,该反应的离子方程式为
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省武汉市、黄陂一中高二下期末化学试卷(解析版) 题型:选择题
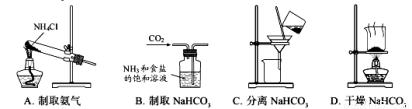
根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取Na HCO3、分离NaHCO3、干燥NaHCO3四个步骤,下列图示装置和原理能达到实验目的的是 ( )
HCO3、分离NaHCO3、干燥NaHCO3四个步骤,下列图示装置和原理能达到实验目的的是 ( )
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省广安市邻水等高一下学期期末联考化学试卷(解析版) 题型:推断题
A、B、C、D、E、F六种元素的原子序数依次递增。已知:
①F的原子序数为29,其余均为短周期主族元素;
②A的内层电子总数是最外层电子数的一半;
③C、E同主族且C原子最外层电子数是次外层电子数的3倍;
④D是金属性最强的短周期元素。完成下列问题
(1)F在元素周期表的位置______________。
(2)B、C、D、E的原子半径由小到大顺序是_________ (用元素符号表示)。
(3)已知D在C的单质中燃烧生成淡黄色的固体化合物甲,甲的化学式为_______________,电子式为_______,甲中的化学键类型为____________________。
(4)A的单质与E的最高价含氧酸反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省广安市邻水等高一下学期期末联考化学试卷(解析版) 题型:选择题
下列叙述错误的是
A.NH3的喷泉实验说明氨气极易溶于水
B.NO 和NH3均可用排空气法收集
C.盛液溴的瓶内加少量水可防止液溴的挥发
D.NH3遇到挥发性的强酸能冒白烟
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省广安市邻水等高一下学期期末联考化学试卷(解析版) 题型:选择题
下列不属于取代反应的是
A.用日光照射甲烷与氯气的混合气体
B.乙烯通入溴水中
C.在FeBr3作催化剂的条件下,苯与液溴反应
D.乙醇与乙酸的酯化反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省广安市邻水等高二下学期期末联考化学试卷(解析版) 题型:填空题
物质在水中可能存在电离平衡、盐的水解平衡和沉淀溶解平衡。根据所学知识回答下列问题:
(1)下列方法中,可以使0.10 mol/L CH3COOH溶液中值增大的措施是___________。
a.加水稀释
b.加入少量CH3COONa固体
c.加入少量冰醋酸
d.通入少量HCl气体
(2)t℃时,水的离子积常数Kw=1×10-12。
①该温度下,若100体积pH=a的H2SO4溶液与1体积pH=b的NaOH溶液混合后溶液呈中性,则a+b= 。
②该温度下,pH=2的某酸HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。试分析其原因 ;该混合溶液中:c(A-)-c(Na+)= mol/L。(填准确数值)
(3)常温下,有浓度均为0.1mol/L的三种溶液:a.NaHCO3;b.NaClO;c.CH3COONa。
①三种溶液pH由大到小的顺序为: (填序号)。
②溶液a的pH大于8,则溶液中c(H2CO3) c(CO32-) (填“>”、“<”或“=”)。
(4)已知25℃ 时,Ksp[AgCl]=1.8×10-10,现将足量氯化银分别放入:a.100mL蒸馏水中;b.100mL 0.2 mol/LAgNO3溶液中;c.100mL 0.1 mol/L氯化铝溶液中;d.100mL 0.1 mol/L盐酸溶液中。充分搅抖后,相同温度下银离子浓度由大到小的顺序是 。 (填写序号);b中氯离子的浓度为 mol/L。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省宿迁市高一下期末化学试卷(解析版) 题型:简答题
综合利用CO2、CO对构建低碳社会有重要意义。
(1)利用H2 和CO在一定条件下发生如下反应:CO(g)+2H2(g) CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。
CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。
①10min后达到平衡时CO的浓度为 ;
②10min内用H2表示的平均反应速率为 ;
③若要加快CH3OH的生成速率,可采取的措施有 (填一种合理的措施)
(2)利用H2 和CO2在一定条件下可以合成乙烯:6H2+2CO2 CH2=CH2+4H2O
CH2=CH2+4H2O
①已知:4.4gCO2与H2完全转化为CH2=CH2和水(气态)共放出6.39kJ的热量,写出该反应的热化学方程式 。
②不同温度对CO2的转化率及催化剂的催化效率的影响如图甲所示。
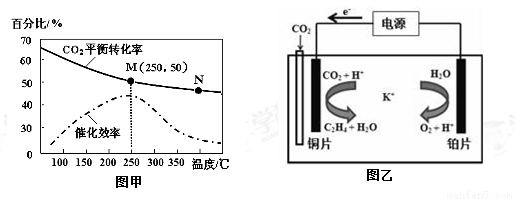
下列有关说法不正确的是 (填序号)。
A.不同条件下反应,N点的速率最大
B.温度在约250℃时,催化剂的催化效率最高
C.相同条件下,乙烯的产量M点比N高
③若在密闭容器中充入体积比为 3∶1的 H2和CO2,则图甲中M点时,产物CH2=CH2的体积分数为 。(保留两位有效数字)
(3)利用一种钾盐水溶液作电解质,CO2电催化还原为乙烯,如图乙所示。在阴极上产生乙烯的电极反应方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省淄博市高二下期末化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是( )
A.铝粉投入到NaOH溶液中:2Al+2OH-+2H2O══ 2AlO2-+3H2↑
B.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓
C.三氯化铁溶液中加入铁粉: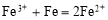
D.FeCl2溶液跟Cl2反应:Fe2++Cl2=Fe3++2Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com