
| A.2 mol | B.2.5 mol | C.3 mol | D.4 mol |
科目:高中化学 来源:不详 题型:单选题
| A.水溶液呈中性 |
| B.与硫酸反应产生1mol氯气时转移2mol电子 |
| C.水溶液不能使淀粉-KI试纸变蓝 |
| D.既含离子键又含共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.第①步当2v(Cr2O72-)=v(CrO42-)时,达到了平衡状态 |
| B.对于上述平衡,加入适量稀硫酸后,溶液颜色变黄色,则有利于CrO42-的生成 |
| C.第②步中,还原0.1 mol Cr2O72-需要45.6 g FeSO4 |
| D.第③步沉淀剂a可以使用NaOH等碱性物质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.电解时发生反应的化学方程式为2HCl Cl2↑+H2↑ Cl2↑+H2↑ |
| B.由NaClO2溶液制取0.6 mol ClO2时,至少消耗0.1 mol NCl3 |
| C.将产生的混合气体通过盛有碱石灰的干燥器以除去ClO2中的NH3 |
| D.溶液X的主要成分为NaClO2和NaOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.开始加入合金的质量可能为16.4 g |
| B.参加反应的硝酸的物质的量为0.1 mol |
| C.生成沉淀完全时消耗NaOH溶液的体积为100 mL |
| D.标准状况下产物NO的体积为22.4 L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Fe(OH)3+5OH-]
Fe(OH)3+5OH-]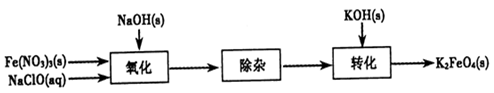
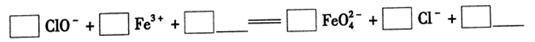
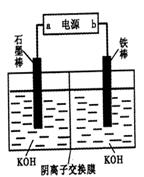
 4Fe(OH)3+8OH-+3O2。实验测得K2FeO4溶液浓度与温度和pH的关系分别如下图所示:
4Fe(OH)3+8OH-+3O2。实验测得K2FeO4溶液浓度与温度和pH的关系分别如下图所示: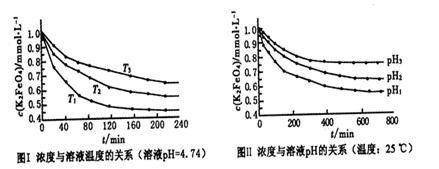
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.化学方程式中产物分子的化学计量数由小到大的顺序是SO2、N2、NH3、H2O |
| B.氧化产物和还原产物的物质的量之比为3∶1 |
| C.被氧化元素原子和被还原元素原子的物质的量之比为2∶3 |
| D.若反应生成1 mol H2O,则转移的电子为6 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
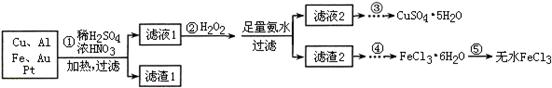
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液(mL) | 25.00 | 25.02 | 26.20 | 24.98 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2H2↑+O2↑,下列有关判断正确的是
2H2↑+O2↑,下列有关判断正确的是| A.氧化剂是氢元素 |
| B.还原产物是O2 |
| C.H2O既有氧化性也有还原性 |
| D.2molH2O反应,转移了8mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com