
(1)钠镁铝三种元素中第一电离能最大的是 。
(2)某正二价阳离子核外电子排布式为[Ar]3d54s0,该金属的元素符号为 。
(3)微粒间存在非极性键、配位键、氢键及范德华力的是 。
A. NH4Cl晶体 B. Na3AlF6晶体 C. Na2CO3•10H2O晶体
D. CuSO4溶液 E. CH3COOH溶液
(4)部分共价键键能数据如下表:
| 键 | H-H | N-H | N-N | N=N | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 159 | 418 | 945 |
根据上表数据推算并写出由氮气和氢气合成氨气的热化学方程式: 。
(5)乙醇和乙醚是同分异构体,但它们性质存在差异:
| 分子式 | 结构简式 | 熔点 | 沸点 | 水溶性 | |
| 乙醇 | C2H6O | C2H5OH | -114.3℃ | 78.4 °C | 互溶 |
| 二甲醚 | C2H6O | CH3OCH3 | -138.5℃ | -24.9℃ | 微溶 |
乙醇和二甲醚沸点及水溶性差异的主要原因是 。
(6)金属铜溶于在浓氨水与双氧水的混合溶液,生成深蓝色溶液。该深蓝色的浓溶液中加入乙醇可见到深蓝色晶体析出,请画出呈深蓝色的离子的结构简式 。
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
将Fe和Cu的混合粉末加入到100 mL 4 mol/L稀硝酸中充分反应后:
(1)若反应后有Cu剩余,则此溶液中一定有的阳离子是__________,可能有的阳离子是_______。(不考虑水电离出的H+,下同)
(2)若反应后的溶液中有Fe3+,则溶液中一定含有的阳离子是________,可能含有的阳离子是______。
(3)如果反应后的溶液中无金属剩余,则加入金属粉末的最大质量应小于_____ ___。
___。
(4) 如果加入的Fe和Cu的质量比为7∶8,则使HNO3完全反应的金属粉末的最小质量为________。
如果加入的Fe和Cu的质量比为7∶8,则使HNO3完全反应的金属粉末的最小质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,错误的是 ( )
A.只含非极性键的纯净物一定是单质
B.只含极性键的纯净物一定是化合物
C.只含离子键的纯净物一定存在金属元素
D.纯净物中一定存在化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素A、B、C、D的原子序数依次递增,最
外层电子数之和为14,A、C同主族,B、D也同主族,A、B在不同周期,X、Y均是由A、B、C、D四
种元素组成的盐,X与Y相互作用,产生气体Z。下列说法正确的是 ( )
A.四种元素形成的简单离子半径按照D、C、B、A的顺序逐渐减小
B.A与其它元素形成的二元化合物的晶体类型相同
C.Z气体通入BaCl2溶液中无现象,再滴入FeCl3溶液则可看到有沉淀产生
D.将Z通入紫色石蕊试液中,试液先变红后褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于σ键和π键的理解不正确的是 ( )
A.σ键能单独形成,而π键一定不能单独形成
B.σ键可以绕键轴旋转,π键一定不能绕键轴旋转
C.双键中一定有一个σ键,一个π键,三键中一定有一个σ键,两个π键
D.气体单质中一定存在σ键,可能存在π键
查看答案和解析>>
科目:高中化学 来源: 题型:
氯水中存在多种微粒,下列有关粒子的表示方法正确的是 ( )
A.氯气的电子式:
B.氢氧根离子的电子式:
C.次氯酸分子的结构式:H—O—Cl
D.HClO的电子式:
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
Cu (s)+2H+ (aq)=Cu2+(aq)+ H2 (g) △H 1
2H2O2(l)=2H2O(l) + O2 (g) △H 2
2H2 (g) + O2 (g)=2H2O(l) △H 3
则反应 Cu (s)+H2O2(l)+2H+ (aq)=Cu2+(aq)+ 2H2O(l) 的△H是
A.△H=△H 1+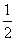 △H 2+
△H 2+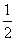 △H 3 B.△H=△H 1+
△H 3 B.△H=△H 1+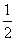 △H 2-
△H 2-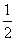 △H 3
△H 3
C.△H=△H 1+2△H 2+2△H 3 D.△H=2△H 1+△H 2+△H 3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与有机物结构、性质相关的叙述错误的是( )
A.乙酸分子中含有羧基,可与NaHCO3溶液反应生成CO2
B.蛋白质和油脂都属于高分子化合物,一定条件下都能水解
C.甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同
D.苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com