
| A. | NaHCO3═Na++HCO3- | B. | NaHSO4═Na++H++SO42- | ||
| C. | HCO3-+H2O?H3O++CO32- | D. | H3PO4?3H++PO43- |
分析 先判断强弱电解质,强电解质完全电离,电离方程式用等号,弱电解质部分电离,电离方程式用可逆号;注意弱电解质的电离分步进行,电离方程式需要分步书写,主要写出第一步的电离即可,据此进行解答.
解答 解:A.碳酸氢钠为强电解质,在溶液中完全电离,其电离方程式为:NaHCO3═Na++HCO3-,故A正确;
B.硫酸氢钠为强电解质,在溶液中完全电离出钠离子、氢离子和硫酸根离子,其电离方程式为:NaHSO4═Na++H++SO42-,故B正确;
C.碳酸氢根离子在溶液中电离出氢离子和碳酸根离子,其电离方程式为:HCO3-+H2O?H3O++CO32-,故C正确;
D.磷酸为弱电解质,电离方程式分别书写,主要以第一步为主,正确的电离方程式为:H3PO4?H++H2PO4-,故D错误;
故选D.
点评 本题考查了电离方程式的书写方法,题目难度不大,明确电离方程式的书写原则为解答关键,试题侧重基础知识的考查,培养了学生的规范答题能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用 HNO2溶液作导电性实验,灯光较暗,说明 HNO2是弱电解质 | |
| B. | NaCl 溶液和 CH3COONH4溶液均显中性,两溶液中水的电离程度相同 | |
| C. | 25℃时,用醋酸溶液中和等浓度 NaOH 溶液至 pH=7,VCH3COOH<VNaOH | |
| D. | AgCl 易转化为 AgI 沉淀且 Ksp(AgX)=[Ag+]•[X-],故 Ksp(AgI)<Ksp(AgCl) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
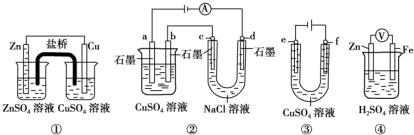
| A. | 装置①中,盐桥中的K+移向CuSO4溶液 | |
| B. | 装置②中b极析出6.4 g固体时,d极产生2.24 L H2 | |
| C. | 用装置③精炼铜时,f极为粗铜 | |
| D. | 装置④中电子沿导线由Zn流向Fe,Fe极上有大量气泡生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、HCO3-、NO3- | B. | Na+、SO42-、Cl-、S2- | ||
| C. | NH4+、Mg2+、SO42-、NO3- | D. | H+、K+、Na+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂能加快反应 | B. | 升高温度能增大反应的速率 | ||
| C. | 改变压强对反应速率没有影响 | D. | 降低温度能加快反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com