
����Ŀ�������ӹ���ķ�����Һ�к�2%��3%��NaNO2������һ�ֻ�����Ⱦ�������NH4Cl��Һ������������Һ��ʹNaNO2ת��Ϊ�����ʣ��÷�Ӧ���������У�
��һ����NaNO2+NH4Cl=NaCl+NH4NO2
�ڶ�����NH4NO2=N2��+2H2O
���жԵڶ�����Ӧ����������ȷ����
��NH4NO2ֻ�������� ��NH4NO2ֻ�ǻ�ԭ��
��NH4NO2�����˷ֽⷴӦ ��ֻ�е�Ԫ�صĻ��ϼ۷����˱仯
��NH4NO2�������������ǻ�ԭ��
A. �٢� B. �٢� C. �ڢۢ� D. �ۢܢ�
���𰸡�D
�����������⿼��������ԭ��Ӧ�Ļ�������ڶ�����Ӧ��NH4NO2������������������ԭ��Ӧ�����е�Ԫ�ط����˹��з�Ӧ��NH4NO2�������������ǻ�ԭ�������Ĵ������Ӧ���Ϳ���NH4NO2�������ǷֽⷴӦ�������ۢܢ�����ȷ�ġ���Dѡ��������⡣
�����͡���ѡ��
��������
16
����Ŀ����ͼ��ʾAlCl3��Һ��NaOH��Һ��μӻ�ϣ���ͼ���жϴ�����ǣ� ��
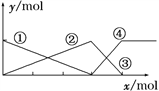
A. ���߱�ʾAl3+���ʵ����ı仯
B. x��ʾAlCl3�����ʵ���
C. ���߱�ʾAl(OH)3���ʵ����ı仯
D. ���߱�ʾAlO![]() ���ʵ����ı仯
���ʵ����ı仯
���𰸡�B
���������ٶ�����1molAlCl3��Һ�еμ�NaOH��Һ�����ȷ�����ӦAl3++3OH-=Al(OH)3����Al3+��ȫ����������3molOH-������1molAl(OH)3��Ȼ������ӦAl(OH)3+OH-=AlO2-+2H2O��������ȫ�ܽ�����1molOH-������1molAlO2-��ǰ�����������ĵ�OH-Ϊ3��1���ٶ�����4molNaOH��Һ�еμ�AlCl3��Һ�����ȷ�����ӦAl3++4OH-=AlO2-+2H2O��OH-��ȫ��Ӧ����1molAl3+������1molAlO2-��Ȼ������ӦAl3++3AlO2-+6H2O=4Al(OH)3����AlO2-��ȫ��Ӧ������![]() molAl3+������
molAl3+������![]() molAl(OH)3����ǰ�����������ĵ�Al3+Ϊ1mol��
molAl(OH)3����ǰ�����������ĵ�Al3+Ϊ1mol�� ![]() mol=3��1����ͼ���֪���٢ڱ�ʾ�����ܱۢ�ʾ�����ʵ�����ϵΪ1��1��֪����ͼ��ʾ��AlCl3��Һ�еμ�NaOH��Һ��A��������������֪�����ȷ�����ӦAl3++3OH-=Al(OH)3������Һ�����������ʵ������٣����߱�ʾAl3+�����ʵ����ı仯��ѡ��A��ȷ��B��������������֪��x��ʾNaOH��Һ��ѡ��B����C��������������֪���淴Ӧ����Al(OH)3���ʵ��������������С���ʢڢ��߱�ʾAl(OH)3�����ʵ����ı仯��ѡ��C��ȷ��D��������������֪��Al(OH)3�ܽ�ʱ��AlO2-�����ʵ��������߱�ʾAlO2-�����ʵ����ı仯��ѡ��D��ȷ����ѡB��
mol=3��1����ͼ���֪���٢ڱ�ʾ�����ܱۢ�ʾ�����ʵ�����ϵΪ1��1��֪����ͼ��ʾ��AlCl3��Һ�еμ�NaOH��Һ��A��������������֪�����ȷ�����ӦAl3++3OH-=Al(OH)3������Һ�����������ʵ������٣����߱�ʾAl3+�����ʵ����ı仯��ѡ��A��ȷ��B��������������֪��x��ʾNaOH��Һ��ѡ��B����C��������������֪���淴Ӧ����Al(OH)3���ʵ��������������С���ʢڢ��߱�ʾAl(OH)3�����ʵ����ı仯��ѡ��C��ȷ��D��������������֪��Al(OH)3�ܽ�ʱ��AlO2-�����ʵ��������߱�ʾAlO2-�����ʵ����ı仯��ѡ��D��ȷ����ѡB��


 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A. ����Ͷ�뵽NaOH��Һ�У�2Al+2OH���T2AlO2��+3H2��
B. AlCl3��Һ�м��������İ�ˮ��Al3++ 3OH�� �TAl(OH)3��
C. ���Ȼ�����Һ�м������ۣ� ![]()
D. FeCl2��Һ��Cl2��Ӧ��2Fe2++Cl2�T2Fe3++2Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ֶ���������Ԫ��aX��bY��cZ����֪a+c=2b����Z������������Ӧ��ˮ��������ѧ������ǿ�ᣬ�������й�˵������ȷ���ǣ� ��
A.��XΪO����Y��X�γɵij���������һ�������ӻ�����
B.��X��Na����Z���������һ����ż��
C.��YΪO����ǽ����ԣ�X��Y��Z
D.��YΪNa����X��Z��������ͬһ����Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ơ��صĵ⻯���������Ϳ�ѧʵ������ʮ����Ҫ��Ӧ�ã���ҵ���õ⡢NaOH����мΪԭ�Ͽ������⻯�ƣ�������������ͼ1�� 
��1��NaOH��Һ�͵ⷴӦʱ��Ҫ�ϸ�����¶ȣ�����¶ȹ��ͣ������ɵ�ĵͼ۸���ƷNaIO����NaOH��Һ�͵ⷴӦʱ������Һ��IO3����IO�������ʵ���֮��Ϊ1��1����÷�Ӧ�����ӷ���ʽΪ ��
��2�����������м��������м��Ŀ���� �� �������ù����г�ʣ����м�⣬���к��ɫ���壬�������мʱ������Ӧ�Ļ�ѧ����ʽ�� ��
��3����Һ2�г�����H+�⣬һ�����е����������������ʵ��֤ʵ�ý��������ӵĴ��� ��
��4����Һ2��һϵ��ת�����Եõ������������壨FeC2O42H2O������ȡ3.60g�����������壨��Է���������180�������ط���������ȷֽ⣬�õ�ʣ�������������¶ȱ仯��������ͼ2��ʾ������ͼ�����ݣ�������Ϣд�����̢���2�Ļ�ѧ����ʽ ��
��300��ʱʣ�����ֻ��һ�����������������ͨ������ȷ����������Ļ�ѧʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���мס��ҡ����������ֽ����������Ƿֱ�Ͷ�뵽��ͬ��ϡ�����У�ֻ�б������ı��������ݲ������ұ����������ݱȶ��죻�ٽ���Ͷ�뵽������Һ�У��ҵı����м������������ֽ����Ļ��˳����ȷ���ǣ� ��
A.�ף��ң�������
B.���������ң���
C.���������ף���
D.���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������KMnO4��Һ���ܴﵽԤ��Ŀ�ĵ���
A.���𱽺ͼױ�
B.������������Һ���Ƿ�����������
C.����CH2=CHCHO�к�̼̼˫��
D.����SO2��CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��鷴Ӧ�й��������ıȽ���ȷ���ǣ� ��
��H2��g��+Cl2��g��=2HCl��g����H1�� ![]() H2��g��+
H2��g��+ ![]() Cl2��g��=HCl ��g����H2����H1����H2
Cl2��g��=HCl ��g����H2����H1����H2
��2H2O��l��=2H2��g��+O2��g����H1�� 2Na��s��+2H2O��l��=2NaOH��aq��+H2��g����H2����H1����H2
��CH3OH��g��+ ![]() O2��g��=CO2��g��+2H2O��l����H1��CH3OH��l��+
O2��g��=CO2��g��+2H2O��l����H1��CH3OH��l��+ ![]() O2��g��=CO2��g��+2H2O��g����H2����H1����H2
O2��g��=CO2��g��+2H2O��g����H2����H1����H2
��t��ʱ����һ�������£��� 1mol N2�� 3mol H2 �ֱ����ں��ݺͺ�ѹ�������ܱ������У��ﵽƽ��״̬ʱ�ų��������ֱ�Ϊ Q1��Q2�� Q1��Q2 ��
A.�٢ۢ�
B.�٢ڢ�
C.�ڢۢ�
D.�٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⻯�ƣ�CaH2�������ǵ�ɽ�˶�Ա���õ���Դ�ṩ����ij��ȤС����ѡ������װ���Ʊ��⻯�ƣ�ԭ��Ϊ��H2+Ca ![]() CaH2�����������Ͽ�֪��
CaH2�����������Ͽ�֪��
�ٸ�����ˮ��Ӧ���ɼ������
���⻯��Ҫ�ܷⱣ�棬�Ӵ���ˮ�ͷ�Ӧ�����������ƺ�����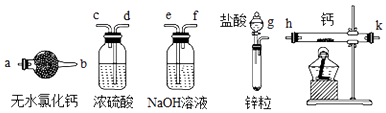
��ش��������⣺
��1���������װ����ѡ����ʵ�װ�ý���ʵ�飬�밴������������˳��g������������k��a���������ӿڵ���ĸ��ţ���
��2��д����ʵ�����Ʊ����������ӷ���ʽ����������ת�Ƶķ������Ŀ
��3����ˮ�Ȼ��Ƶ������� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com