
分析 (1)X为H2S,H2S在空气中变浑浊是因为被氧气氧化为S;
(2)Na2S2O3中S为+2价,从氧化还原的角度分析,反应物中S元素化合价必须分别大于2和小于2;
(3)由原子和元素守恒可知,缺项为水,结合电子、原子守恒配平;
(4)硫代硫酸钠与稀硫酸反应生成了单质硫,溶液变浑浊,反应速率越快,出现浑浊时间越短;
(5)反应每得到1mol硫,放出270kJ的热量,以此书写热化学方程式;
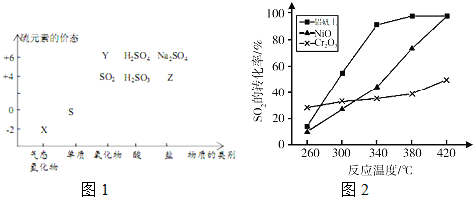
(6)由图可知,相同条件下铝钒土作催化剂时,二氧化硫的转化率最大.
解答 解:(1)X为H2S,H2S在空气中变浑浊是因为被氧气氧化为S,反应的化学方程式为2H2S+O2=2S↓+2H2O,故答案为:2H2S+O2=2S↓+2H2O;
(2)Na2S2O3中S为+2价,从氧化还原的角度分析,反应物中S元素化合价必须分别大于2和小于2,a中S化合价都小于2,c中S的化合价都大于2,bd符合题意,
故答案为:bd;
(3)由原子和元素守恒可知,缺项为水,反应中S元素的化合价由+6价降低为+4价,S元素的化合价由0升高为+4价,结合电子、原子守恒可知反应为4KAl(SO4)2•12H2O+3S$\frac{\underline{\;高温\;}}{\;}$2K2SO4+2Al2O3+9SO2↑+48H2O,故答案为:4;3;2;2;9;48H2O;
(4)根据硫代硫酸钠与稀硫酸反应生成了单质硫,溶液变浑浊,可以判断反应速率快慢,反应速率越快,出现浑浊时间越短,
故答案为:b;
(5)反应每得到1mol硫,放出270kJ的热量,热化学方程式为2CO(g)+SO2(g)$\frac{\underline{\;铝钒土\;}}{380℃}$S(l)+2CO2 (g)△H=-270kJ/mol,
故答案为:2CO(g)+SO2(g)$\frac{\underline{\;铝钒土\;}}{380℃}$S(l)+2CO2 (g)△H=-270kJ/mol;
(6)由图可知,生产中选铝钒土做催化剂的主要原因是铝钒土作催化剂,在相对较低温度下,单位时间内获得较高的SO2转化率,能耗小,
故答案为:铝钒土作催化剂,在相对较低温度下,单位时间内获得较高的SO2转化率,能耗小.
点评 本题考查较综合,涉及非金属性比较、氧化还原反应、反应速率及热化学方程式等,侧重反应原理中高频考点的考查,综合性较强,题目难度不大.


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:选择题
| A. | 吸收183kJ | B. | 吸收284kJ | C. | 放出183kJ | D. | 放出 248kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “煤的液化”是指将煤加热变为液态 | |
| B. | “乙醇汽油”是为了增大燃烧的热值,在汽油中加入乙醇 | |
| C. | 光伏发电要用到铟,该元素是一种副族的金属元素 | |
| D. | 将燃料的燃烧反应设计为原电池,可以提高能量的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气和水的反应:C12+H2O=2H++Cl-+ClO- | |
| B. | 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3•H2O+H2O | |
| C. | 碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O | |
| D. | 硫酸与氢氧化钡溶液反应:Ba2++OH-+SO42-+H+=BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为向100mL 2mol/L AlCl3溶液中加入2mol/L NaOH溶液过程中,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线.试回答:
如图为向100mL 2mol/L AlCl3溶液中加入2mol/L NaOH溶液过程中,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫酸钡为强酸强碱的难溶性盐,俗名叫重晶石.
硫酸钡为强酸强碱的难溶性盐,俗名叫重晶石.| 反应温度 | 300℃ | 400℃ | 500℃ | 600℃ | 700℃ |
| 平衡常数 | 3.8 | 5.7 | 8.5 | 9.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8:1 | B. | 2:1 | C. | 1:1 | D. | 1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物种类相同 | |
| B. | 由苯制取溴苯、硝基苯、环己烷的反应类型均属于取代反应 | |
| C. | 乙烷、苯、葡萄糖溶液均不能使酸性高锰酸钾溶液褪色 | |
| D. | 乙酸乙酯、乙酸、乙醇均能和水互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱、Na2O2、NH4NO3、Ca(OH)2均为离子化合物 | |
| B. | HCl、H2SO4、HNO3均具有氧化性,都是氧化性酸 | |
| C. | 经分析某物质只含有一种元素,则该物质一定是纯净物 | |
| D. | 金属氧化物一定是碱性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com