
(8分) HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;7在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________(填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是________(填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:________________________ 。
(4) Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________(填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
(每空2分,共8分)(1) D (2) B
(3) NO2- + Cl2 + H2O = NO3- +2 Cl- + 2 H+ (4)c
【解析】
试题分析:(1)根据题意可知误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒,说明亚硝酸钠是氧化剂,把亚铁离子氧化为铁离子,本身被还原,而维生素C是还原剂,又把铁离子还原为亚铁离子。所以答案选D;
(2)A、亚硝酸是弱酸,则亚硝酸钠是强碱弱酸盐,溶液呈碱性,而氯化钠溶液呈中性,可以用pH鉴别,正确;B、甲基橙的变色范围是3.1~4.4,大于4.4,溶液呈黄色,亚硝酸钠与氯化钠的溶液的pH都大于4.4,溶液均为黄色,所以不能用甲基橙鉴别,错误;C、亚硝酸钠具有氧化性,可以氧化碘离子为碘单质,溶液变蓝色,而氯化钠不能使KI—淀粉溶液变蓝色,可以鉴别,正确;D、氯化钠与硝酸银溶液反应生成氯化银白色沉淀,而亚硝酸钠与硝酸银溶液不反应,可以鉴别,正确,答案选B。
(3)根据实验现象可知,氯水褪色,说明氯水中的氯气与亚硝酸钠发生了氧化还原反应,根据生成的产物判断,氯气是氧化剂,亚硝酸钠是还原剂,实验发生的离子方程式为NO2- + Cl2 + H2O = NO3- +2 Cl- + 2 H+;
(4)将亚铁离子氧化为铁离子,同时又不能引入其他杂质,氯气会引入氯离子,Fe不能氧化亚铁离子,硝酸会引入硝酸根离子,只有过氧化氢作氧化剂时,还原产物是水,不会引入其他离子,答案选c。
考点:考查物质氧化性、还原性的判断,亚硝酸钠的化学性质应用,离子方程式的书写,氧化剂的选择


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届山东省高三上学期第二次检测化学试试卷(解析版) 题型:选择题
下列实验装置、选用的试剂或实验操作中,都正确的是
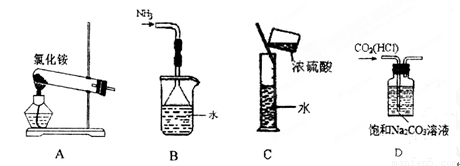
A.实验室用装置A制取氨气 B.用B装置吸收氨气,并防止倒吸
C.用C装置稀释浓硫酸 D.用D装置除去CO2中的HCl
查看答案和解析>>
科目:高中化学 来源:2015届山东省文登市高三上学期11月月考化学试卷(A卷)(解析版) 题型:选择题
根据表中信息,判断下列叙述中正确的是
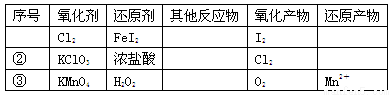
A.表中①组的反应中氧化产物一定是I2
B.氧化性强弱的比较:KClO3>Cl2>Fe3+>I2
C.表中②组每生成1molCl2,转移1mol电子
D.表中③组其他反应物可以为浓盐酸
查看答案和解析>>
科目:高中化学 来源:2015届山东省德州市高三期中考试化学试卷(解析版) 题型:选择题
已知:①Na3N+3H2O===3NaOH+NH3↑,②NaH+H2O===NaOH+H2↑下列叙述正确的是
A.离子半径:N3->Na+>H+
B.反应①和②都是氧化还原反应
C.反应①和②氧化剂都是H2O
D.Na3N和NaH与盐酸反应都只生成一种盐
查看答案和解析>>
科目:高中化学 来源:2015届山东省德州市高三期中考试化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.1H、D+、T2互为同位素
B.H2O、CH3COOH、NH4HCO3都是电解质
C.铝、铁、铜三者对应的氧化物均为碱性氧化物
D.有单质参加的反应一定是氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2015届山东省德州市高三10月月考化学试卷(解析版) 题型:选择题
已知: ①向KMnO4溶液中滴加浓盐酸,产生黄绿色气体; ②向KBr溶液中通入少量实验①产生的气体,溶液变黄色; ③取实验②生成的溶液少量滴在FeCl2与KSCN的混合溶液中,溶液变血红色。根据以上实验,下列判断正确的是
A.上述实验中,共有两个氧化还原反应
B.上述实验证明还原性:Fe2+>Br->Cl-> Mn2+
C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝
D.实验③证明Fe2+既有氧化性又有还原性
查看答案和解析>>
科目:高中化学 来源:2015届山东省德州市高三10月月考化学试卷(解析版) 题型:选择题
下列是某同学对相应的离子方程式所作的评价,其中评价合理的是
编号 | 化学反应 | 离子方程式 | 评 价 |
A | 碳酸钙与醋酸反应 | CO32-+2CH3COOH =CO2↑+H2O+2CH3COO- | 错误,碳酸钙是弱电解质,不应写成离子形式 |
B | NaAlO2溶液中通入过量CO2 | 2AlO2-+CO2+3H2O==2Al(OH)3↓+CO32- | 正确 |
C | NaHCO3的水解 | HCO3-+H2O ═ CO32-+H3O+ | 错误,水解方程式误写成电离方程式 |
D | 等物质的量的FeBr2和Cl2反应 | 2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | 错误,离子方程式中Fe2+与Br-的物质的量之比与化学式不符 |
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第一次模拟考试试卷(解析版) 题型:选择题
可以大量共存的离子组是
A.Na+、Fe2+、NO3-、C1- B.K+、HCO3-、SO42-、OH-
C.C1O-、C1-、Na+、H+ D.Ba2+、K+、SO42-、H+
查看答案和解析>>
科目:高中化学 来源:2015届山东省乐陵市高三10月初检测化学试卷(解析版) 题型:选择题
某混合气体G可能含有CO、CO2、SO2、H2O等气体,用a.无水CuSO4、b.澄清石灰水、c.灼热CuO、d.碱石灰、e.品红溶液、f..酸性高锰酸钾溶液等药品可将其一一检出,检出的正确顺序是……( )
A.G→a→e→b→f→d→c B.G→c→d→b→e→f→a
C.G→a→e→f→b→d→c D.G→b→e→f→a→d→c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com