
科目:高中化学 来源: 题型:选择题
| A. | 强碱溶液会腐蚀光导纤维 | |
| B. | 硅是良好的半导体,是信息技术的关键材料 | |
| C. | 碳化硅具有金刚石结构,硬度大,可以作砂轮的磨料 | |
| D. | 水晶镜片所用原料为晶体硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素、油脂都属于高分子化合物 | |
| B. | 天然蛋白蛋水解的最终产物均是氨基酸 | |
| C. | 羧酸能发生酯化反应 | |
| D. | 油脂水解得到的醇是丙三醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干冰升华和液溴挥发 | B. | 金刚石熔化和金属铜熔化 | ||
| C. | 蔗糖溶于水和H2SO4溶于水 | D. | 食盐粉碎和干冰粉碎 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由①可知原溶液存在离子为NH4+,其浓度为0.03mol/L | |
| B. | 原溶液肯定没有Fe3+、Mg2+,一定含有Na+ | |
| C. | n(NH4+):n(Al3+):n(SO42-)=3:1:10 | |
| D. | 原溶液一定存在Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸,并测得某溶液pH为3.1 | |
| B. | 中和pH与体积均相同的NaOH溶液和氨水,结果消耗H2SO4的物质的量一样多 | |
| C. | 酸碱中和滴定的终点是指酸和碱恰好完全反应,此时溶液一定呈中性 | |
| D. | 在HCl气氛中蒸干AlCl3溶液能到得纯净的无水氯化铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
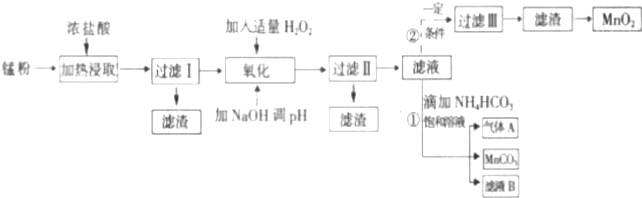
| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | Zn(OH)2 |
| 沉淀开始时pH | 7.5 | 2.2 | 8.8 | 6.5 |
| 沉淀完全时pH | 9.5 | 3.7 | 10.8 | 8.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com