
����Ŀ��ˮ��ҺX��ֻ��������K+ �� Mg2+ �� Al3+ �� AlO2�� �� SiO32�� �� SO32�� �� CO32�� �� SO42���е����������ӣ�ijͬѧ�Ը���Һ��������ͼ��ʾʵ�飺�����ж���ȷ���ǣ� �� 
A.�����һ���Ǵ�����
B.�������ǹ������þ�Ļ����
C.K+ �� AlO2����SiO32��һ����������ҺX��
D.CO32����SO42��һ������������ҺX��
���𰸡�C
���������⣺��HCl������˵����CO32����SO32�� �� �����߶��У����ɵ������Ƕ�����̼������������߶��У�һ�������ں�̼���������������Ӳ���������ӣ����Բ�����þ���ӡ������ӣ��������г�����˵��һ���й�������ӣ������dz��������������ˮ���ṩOH�����г������ɣ�ֻ������������������˵����ʱ��Һ�д��������ӣ�����ԭ����Һ�е�������һ�����ܴ��ڣ����Ը���������ƫ��������Ӻ����ᷴӦ���ɵģ����ԣ�һ������ƫ��������ӣ�Ҫ��֤��Һ�����ԣ�ֻ��K+��һ�������ӣ�����һ�����ڼ����ӣ�
A����HCl������˵����CO32����SO32�� �� ���ɵ������Ƕ�����̼�������������ߵĻ�����壬��A����
B����Һ��һ������CO32����SO32�� �� �����߶��У���һ��������þ���ӣ����Ǻ�þ���Ӷ������棬���Գ������ǹ��ᣬ�������ǹ���þ����B����
C��ԭ����Һ��K+�� ![]() ��
�� ![]() һ�����ڣ���C��ȷ��
һ�����ڣ���C��ȷ��
D������������Ƿ���ڲ���ȷ����CO32�����ܴ��ڣ���D����
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���Ԫ�����ʵĵݱ����������ǣ� ��
A.Li��Be��Bԭ��������������������
B.N��O��F�縺����������
C.P��S��ClԪ�����������������
D.Na��K��Rb��һ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���ѧ����������ᡢ����������ء������й�˵������ȷ����
A.ʳ���ͷ������Ȼ�����������������к�����
B.����������������������
C.�����ڼ�ɾ�����ϡ�ͺ����84������Һ������Ƶ���Ӵ��Ľ����Ű��ֽ���ɱ������
D.�й�������̫��������뮺�밷�����ѧ��Ӧ�������ڶȸ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ơ���������1mol�ֱ�Ͷ�뵽�������ͬŨ�ȵ������У������������������ͬ�����£� ��
A.�ƿ������
B.����������һ����
C.��һ�����
D.���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��XΪһ�ֳ�������������������a��b��c����ѧ��ѧ�������ʣ����ɳ���Ԫ����ɣ�ת����ϵ��ͼ��ʾ������˵������ȷ����
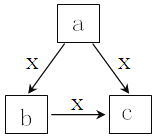
A. ��a��b��c��ɫ��Ӧ���ʻ�ɫ��ˮ��Һ���ʼ��ԣ���a�п��ܼȺ������Ӽ��ֺ��й��ۼ�
B. ��XΪO2��aΪһ�ֹ�̬���ʣ���c����ΪCO2��SO3
C. ��bΪ��̬�ǽ������ʣ�b��X����Ԫ��ͬ���壬��a��b��c������X��Ӧ
D. ��aΪ��̬�ǽ������ʣ�a��X����Ԫ��ͬ���������³�ѹ��cΪ��ɫ���壬��X��a����Ԫ��ԭ�ӵĺ˵�������2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰȫ��Χ�ڻ�����Ⱦ���ܹ�ע������������Ӧ������������ɫ��ѧ������ԭ�Ӿ������������ҵ�����еķ���������Ϊ��Ҫ����ҵ������������ʱ����ͬʱ������һ�ֳ�������Ҫ������������Ư����������(NaClO2)���乤���������£�
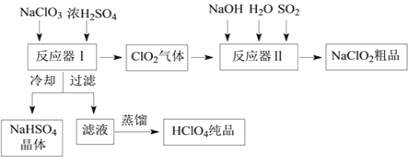
��֪����NaHSO4�ܽ�����¶ȵ����߶������ʵ������¿ɽᾧ�������ڸ�����������Ϊֹ������֪���е���ǿ�ᣬ�е�90������ش��������⣺
��1����Ӧ�����з�����Ӧ�Ļ�ѧ����ʽΪ_______����ȴ��Ŀ����____________��
��2����Ӧ�����з�����Ӧ�����ӷ���ʽΪ__________________________��
��3��ͨ�뷴Ӧ�����е�SO2��H2O2����ͬ��������NaClO2�����Ҫ˵��˫��ˮ�ڷ�Ӧ���ܴ���SO2��ԭ����_________________________��
��4��Ca(ClO)2��ClO2��NaClO2�Ⱥ��Ȼ����ﶼ�dz��õ���������Ư������д����ҵ������������ʯ������Ư�۾��Ļ�ѧ����ʽ��___________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��������������������Ҫ�ɷ�ΪFe2O3��FeO��SiO2�ȣ�Ϊԭ���Ʊ��ߵ�������������(Fe2O3)�����������������£�

�Իش��������⣺
��1��������������ϡ��������ʱ�IJ�����Ϊ______________���ѧʽ����
��2��ʵ����ʵ�����������з���������õIJ���������______________��
��3�����鲽�����Ѿ�������ȫ���Լ���______________��
��4���������ķ�Ӧ�¶�һ���������35�����£���Ŀ����____________________________��
��5���������з�����Ӧ�Ļ�ѧ����ʽΪ______________��
��6�����ⶨ������������FeԪ�ص�������������ȡag��Ʒ�����������������ˮ��������ˣ�����Һ�м���������H2O2����ַ�Ӧ�����NaOH��Һ�����ټ������������������ˡ�ϴ�ӡ�������������أ���ȴ��Ƶò�������bg�� �������Ʒ��FeԪ�ص���������Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.NaOH��Ħ������Ϊ40 g
B.1 mol O2��������������Է����������
C.1 mol OH��������Ϊ17 gmol��1
D.������Ħ����������λgmol��1������ֵ�ϵ����������ԭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ij��ѧ�С�����о���ѧϰ��̽�������Ƿ��ӵ���ɺͽṹʱ��Ʋ���ɵ�һ��ʵ�飺����������Һ��ֱ�ȡ2 mL�Ⱥ�ӵ�2 mL������Cu(OH)2�У������ʵ�������¼�����
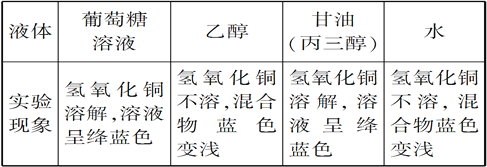
��������ʵ�鼰�����ܹ��ó�����ȷ������(����)
A. �����Ƿ����п��ܺ���ȩ��
B. �����Ƿ����п��ܺ��ж���ǻ�
C. �����ǵķ���ʽΪC6H12O6
D. �����Ƿ���̼���ʾ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com