
【题目】硫酰氯(SO2Cl2)熔点-54.1℃、沸点69.2℃,在染料、药品、除草剂和农用杀虫剂的生产过程中有重要作用。
(1)SO2Cl2中S的化合价为___________,SO2Cl2在潮湿空气中因水解“发烟”的化学方程式为__________。
(2)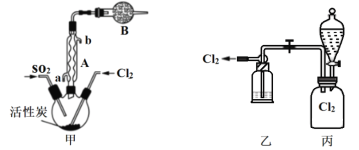
①仪器A的名称为___________,装置B的作用是____________。
②装置乙中装入的试剂是浓硫酸,装置丙分液漏斗中盛装的最佳试剂是________(选填字母)。
A.蒸馏水 B.10.0 molL1浓盐酸 C.浓氢氧化钠溶液 D.饱和食盐水
③滴定法测定硫酰氯的纯度:取1.800g产品,加入到100mL 0.5000mol·L1 NaOH溶液中加热充分水解,冷却后加蒸馏水准确稀释至250mL,取25mL溶液于锥形瓶中,滴加2滴甲基橙,用0.1000mol·L1标准HCl滴定至终点,重复实验三次取平均值,消耗10.00mL滴定终点的判断为___________,产品的纯度为_________。
(3)探究硫酰氯在催化剂作用下加热分解的产物,实验装置如图所示(部分夹持装置未画出)。

①加热时A中试管出现黄绿色,装置B的作用是_________。
②装置C中反应的离子方程式为________。
【答案】+6 ![]() (球形)冷凝管 防止空气中的水蒸气进入三颈瓶,使SO2Cl2水解变质;吸收尾气 D 滴加最后一滴HCl标准液,锥形瓶内溶液由黄色变为橙色且30s内不变色 75.00% 吸收氯气
(球形)冷凝管 防止空气中的水蒸气进入三颈瓶,使SO2Cl2水解变质;吸收尾气 D 滴加最后一滴HCl标准液,锥形瓶内溶液由黄色变为橙色且30s内不变色 75.00% 吸收氯气 ![]()
【解析】
(1)SO2Cl2中O为-2价、Cl为-1价,则S的化合价为+6;SO2Cl2在潮湿空气中因水解“发烟”的化学方程式为![]() ;
;
(2)①仪器A的名称为球形冷凝管;装置B的用处可从两个角度进行分析,一是防止空气内的水进入装置造成反应底物的污染,二是防止反应产物进入空气造成污染;
②氯气不溶于饱和食盐水,通过滴加饱和食盐水,将氯气排除,其他选项均不符合,故选D;
③硫酰氯在NaOH溶液中转化为NaCl和硫酸钠,用盐酸滴定过量的NaOH,甲基橙作指示剂,因此滴定终点的现象为滴加最后一滴HCl标准液,锥形瓶内溶液由黄色变为橙色且30s内不变色;发生的反应为![]() 和
和![]() ,因此
,因此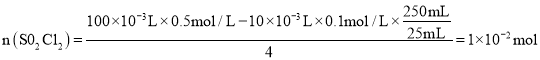 ,则
,则![]() ,故产品的纯度为1.35g÷1.800g×100%=75.00%;
,故产品的纯度为1.35g÷1.800g×100%=75.00%;
(3)硫酰氯分解生成了氯气,Cl的化合价升高,化合价降低的元素只能是S,从+6降到+4,生成二氧化硫。
①加热室A中出现黄绿色,说明生成了氯气,装置B的作用是吸收氯气;
②装置C中的现象是高锰酸钾溶液褪色,二氧化硫将其还原,离子方程式为![]() 。
。


科目:高中化学 来源: 题型:
【题目】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务,回答有关问题:
(1)在一定条件下,2H2O==2H2↑+O2↑,下图能正确表示该反应中能量变化的是________(用A、B表示)。

从断键和成键的角度分析上述反应中能量的变化。化学键的键能如下表:则生成1mol水热量变化为________kJ。
化学键 | H—H | O=O | H—O |
键能kJ/mol | 436 | 496 | 463 |
(2)在生产和生活中经常遇到化学能与电能的相互转化,银锌电池是一种常见化学电源,其反应原理:Zn+Ag2O+H2O=Zn(OH)2+2Ag,其工作示意如图所示。在装置中Ag2O作_______极(填正或负)溶液中的K+向_____电极移动(填“Zn”或“Ag2O”);Ag2O电极发生______(还原或氧化反应),电极反应式为_____________________。
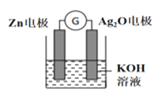
(3)一定温度下,将3molA气体和1molB气体通入一容积固定为1L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为_______;x为_________;此时反应物B的转化率为_________。若反应经2min达到平衡,平衡时C的浓度_____0.8mol/L(填“大于,小于或等于”)。
xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为_______;x为_________;此时反应物B的转化率为_________。若反应经2min达到平衡,平衡时C的浓度_____0.8mol/L(填“大于,小于或等于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室配制480mL 0.2molL﹣1的Na2SO4溶液,实验操作步骤有:
A.在托盘天平上称出________g硫酸钠固体,把它放在烧杯中,用适量的蒸馏水使它完全溶解并冷却至室温。
B.把制得的溶液小心地转移到容量瓶中。
C.继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,改用_______________小心滴加蒸馏水至溶液凹液面最低处与刻度线相切。
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡。
E.将容量瓶瓶塞塞紧,充分摇匀。
请填写下列空白:
(1)操作步骤的正确顺序为(填序号):_______________。
(2)所用硫酸钠固体的质量是___________g。
(3)本实验用到的基本仪器已有烧杯、天平(带砝码、镊子)、玻璃棒、药匙,C步骤空白处的仪器是_________________,还缺少的仪器是____________________。
(4)下列情况会使所配溶液浓度偏高的是(填序号)_______________。
a.定容时俯视刻度线
b.没进行上述的操作步骤D
c.摇匀后发现液面低于刻度线
d.砝码上沾有杂质
e.容量瓶使用前内壁沾有水珠
Ⅱ.掌握仪器名称、组装及使用方法是中学化学实验的基础。
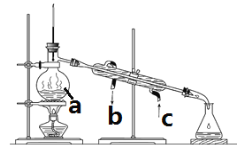
(1)写出仪器a名称:________________
(2)可用该方法分离的组合是____________
a.食盐和沙子
b.硝酸钾和氯化钠的混合溶液
c.四氯化碳和水
d.水和酒精
(3)冷凝水的通向是:_____口进_____口出(填图片上对应的字母)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔在不同条件下可以转化成许多化合物,如图,下列叙述错误的是( )
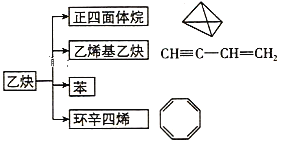
A. 正四面体烷的一氯代物及二氯代物均只有1种
B. 乙炔生成乙烯基乙炔是加成反应
C. 等质量的苯与乙烯基乙炔完全燃烧时的耗氧量不同
D. ![]() 与环辛四稀互为同分异构体,1mol的两种混合物都能最多和4mol H2加成
与环辛四稀互为同分异构体,1mol的两种混合物都能最多和4mol H2加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A、B、C、D、E、F、G有如下转化关系,其中C是最简单的烯烃,G的分子式为C9H10O2,试回答下列有关问题。
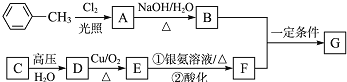
(1)G的名称为_____。
(2)指出下列反应的反应类型:A转化为B:____;C转化为D:___。
(3)写出下列反应的化学方程式:G与足量NaOH溶液反应的化学方程式:____。
(4)符合下列条件的G的同分异构体数目为____种。
①苯环上有3个取代基,且有两个取代基相同;
②能够与新制的银氨溶液反应产生光亮的银镜。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是某同学设计的用于鉴别苯和苯的同系物的几种方法或试剂,其中最适合的是( )
A. 液溴和铁粉B. 浓溴水
C. 酸性KMnO4溶液D. 在空气中点燃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蒽(![]() )与苯炔(
)与苯炔(![]() )反应生成化合物X(立体对称图形),如下图所示:
)反应生成化合物X(立体对称图形),如下图所示:
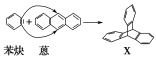
(1)蒽与X都属于________。
a.环烃 b.烃 c.不饱和烃
(2)苯炔的分子式为________,苯炔不具有的性质是________。
a.能溶于水 b.能发生氧化反应
c.能发生加成反应 d.常温常压下为气体
(3)下列属于苯的同系物的是________(填字母)。
A. 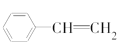
B. 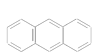
C. 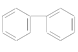
D. ![]()
(4)下列物质中,能发生加成反应,也能发生取代反应,同时能使溴水因加成反应而退色,还能使酸性高锰酸钾溶液退色的是___。
A. ![]()
B.C6H14
C. ![]()
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水是自然界中的淡水经过絮凝、沉淀、过滤、消毒等工艺处理后得到的。常用的自来水消毒剂有二氧化氯(ClO2)和高铁酸钾(K2FeO4)等。
(1)某研究小组用下图装置制备少量ClO2(夹持装置已略去)。
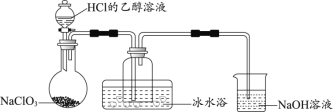
资料:ClO2常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色,11℃时液化成红棕色液体。以NaClO3和HCl的乙醇溶液为原料制备ClO2的反应为2NaClO3 + 4HCl= 2ClO2↑+ Cl2↑+ 2NaCl + 2H2O。
①冰水浴的作用是____________。
② NaOH溶液中发生的主要反应的离子方程式为________________。
(2)将ClO2水溶液滴加到KI溶液中,溶液变棕黄;再向其中加入适量CCl4,振荡、静置,观察到____,证明ClO2具有氧化性。
(3)ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO2-),需将其转化为Cl-除去。下列试剂中,可将ClO2-转化为Cl-的是_____________________(填字母序号)。
a. FeSO4 b. O3 c. KMnO4 d. SO2
(4)K2FeO4是一种新型、绿色的多功能净水剂,集氧化、吸附、絮凝、沉淀、灭菌、消毒、脱色、除臭等性能为一体。实验室制备K2FeO4的方法如下:在冰水浴中,向KClO和KOH的混合溶液中少量多次加入硝酸铁,并不断搅拌。
①上述制备K2FeO4反应的离子方程式为______________________。
②净水过程中,K2FeO4起到吸附、絮凝作用的原理是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究电解质在水溶液中的平衡能了解它的存在形式。
(1)常温下,向100mL0.01molL-1HA的溶液中逐滴加入0.02molL-1MOH溶液,所得溶液的pH随MOH溶液的体积变化如图所示(溶液体积变化忽略不计)。

①常温下,0.01molL-1HA溶液中由水电离出的c(H+)=______molL-1。
②常温下一定浓度的MA稀溶液的pH=a,则a__7(填“>”、“<”或“=”),用离子方程式表示其原因为_______________________________________;
③X点时,溶液中c(H+)、c(M+)、c(A—)由大到小的顺序是___________________;
④K点时,溶液中c(H+)+c(M+)—c(OH—)=____molL-1。
⑵20℃时,在c(H2C2O4)+c(HC2O4—)+c(C2O42—)=0.100molL—1的H2C2O4、NaOH混合溶液中,H2C2O4、HC2O4-、C2O42-的物质的量分数δ随溶液pH变化的关系如图所示。

①Q点:c(H2C2O4)______c(HC2O4—)(填“>”、“<”或“=”)
②该温度下HC2O4-的电离常数K=___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com