
| A.压强 | B.温度 |
| C.催化剂 | D.反应物的性质 |
科目:高中化学 来源:不详 题型:单选题
 2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则( )
2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则( )查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
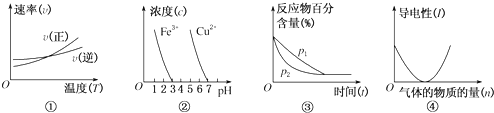
| A.根据图①可判断反应的△H<0 |
| B.根据图②,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5 |
| C.图③可表示压强(p)对反应2A(g)+2B(g)?3C(g)+D(s)的影响 |
| D.图④可表示向醋酸溶液中通入氨气时,溶液导电性随氨气量的变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 |
| D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.催化剂是通过降低反应所需的活化能来增大反应速率的 |
| B.对于有气体参加的反应,压强增大,单位体积内的活化分子数增多,发生有效碰撞的机会增多,反应速率加快 |
| C.发生碰撞的分子只要具有足够的能量,就能够发生有效碰撞 |
| D.光、电磁波、超声波等因素会对反应速率产生影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.加入适量镁粉 | B.加入适量的水 |
| C.加入几滴硫酸铜溶液 | D.再加入少量稀硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.F2+H2=2HF | B.Cl2+H2=2HCl |
| C.Br2+H2=2HBr | D.I2+H2=2HI |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com