
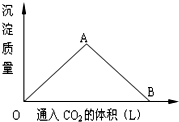
 如图为一定量的饱和Ca(OH)2澄清溶液中通入二氧化碳气体后,产生碳酸钙白色沉淀的质量与通入二氧化碳气体体积的关系曲线,请回答下列问题:
如图为一定量的饱和Ca(OH)2澄清溶液中通入二氧化碳气体后,产生碳酸钙白色沉淀的质量与通入二氧化碳气体体积的关系曲线,请回答下列问题:

科目:高中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
| 压强/Mpa 转化率 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
查看答案和解析>>
科目:高中化学 来源:2012届海南省琼海市嘉积中学高三上学期教学质量监测(一)化学试卷 题型:实验题
(12分)某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示的装置进行有关实验。请回答: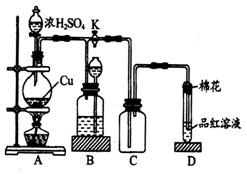
(1)装置A中发生的化学反应方程式为 。
(2)装置D中试管口放置的棉花中应浸一种液体,这种液体是 ,其作用是 。
(3)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是 。B中应放置的液体是 (填字母)。
a. 水 b. 酸性KMnO4溶液 c. 浓溴水 d. 饱和NaHSO3溶液
(4)实验中,取一定质量的铜片和一定体积18mol·L-1的浓硫酸放在圆底烧瓶中共热,直 到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是 。
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是 (填字母)。
a. 铁粉 b. BaCl2溶液 c. 银粉 d. Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
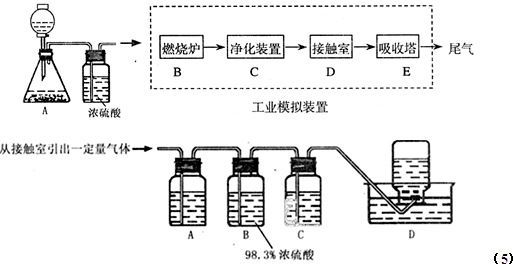
某化学兴趣小组的同学为模拟工业制造硫酸的生产过程,设计了如图所示的装置,请根据要求回答问题:
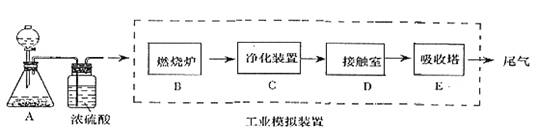
(1)装置A用来制取氧气,写出相应的化学方程式__________________________;
(2)燃烧炉内放一定量黄铁矿粉末,在高温条件下和A装置制出的氧气充分反应,其化学方程式为 ,在该反应中____________做氧化剂,若消耗了12gFeS2有_________mol电子发生了转移;
(3)C装置为净化装置,若无该装置,将混合气体直接通入D装置,除对设备有腐蚀外,还会造成的后果是___________________________________;
(4)如果D装置的温度是400℃~500℃,回答在工业中不采取加压措施的原因_______
______________________________________ ;
(5)为检验从接触室出来的气体成分,甲同学设计如下实验:
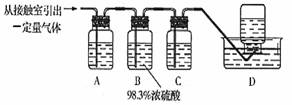
①A中盛放的试剂是____________________;
②B中盛放98.3%浓硫酸的作用是_______________________________________,乙同学提出可用饱和NaHSO3溶液代替98.3%的浓硫酸,请你判断乙同学的方案_ _____(填“可行”或“不可行”)说明理由___________ ;
③C中盛放的试剂是________________,其作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组的同学为模拟工业制造硫酸的生产过程,设计了如图所示的装置,请根据要求回答问题:
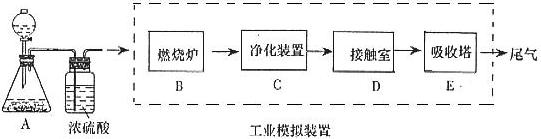
(1)装置A用来制取氧气,写出相应的化学方程式__________________________;
(2)燃烧炉内放一定量黄铁矿粉末,在高温条件下和A装置制出的氧气充分反应,其化学方程式为![]() ,在该反应中____________做氧化剂,若消耗了
,在该反应中____________做氧化剂,若消耗了![]() 有_______________mol电子发生了转移;
有_______________mol电子发生了转移;
(3)C装置为净化装置,若无该装置,将混合气体直接通入D装置,除对设备有腐蚀外,还会造成的后果是_____________________________________________;
(4)如果D装置的温度是400℃~500℃,在常压下生成![]() ,可放出
,可放出![]() 的热量,请写出该反应的热化学方程式__________________________________________;
的热量,请写出该反应的热化学方程式__________________________________________;
并回答在工业中不采取加压措施的原因
__________________________________________________________________;
(5)为检验从接触室出来的气体成分,甲同学设计如下实验:
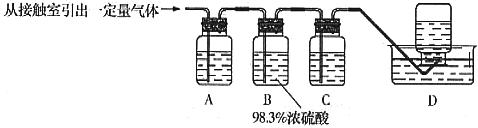
①A中盛放的试剂是____________________;
②B中盛放98.3%浓硫酸的作用是__________________________________________,乙同学提出可用饱和NaHSO3溶液代替98.3%的浓硫酸,请你判断乙同学的方案________(填“可行”或“不可行”)说明理由_________________________________________________
_______________________________;
③C中盛放的试剂是___________________________,其作用是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com