
| A.在化合物中呈+2价 | B.镭比钙的金属性强 |
| C.氢氧化物呈两性 | D.碳酸盐难溶于水 |
科目:高中化学 来源:不详 题型:填空题
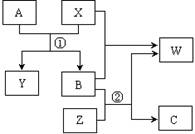
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
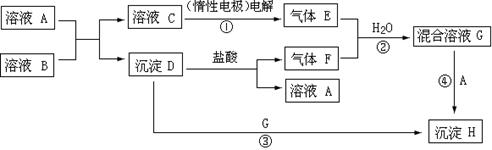
 : n(F)>1:1,则在混合溶液G中滴入几滴石蕊
: n(F)>1:1,则在混合溶液G中滴入几滴石蕊查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

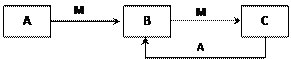 |
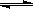 6H2O+5N2。在一定条件下,该反应达到平衡态I后,升高温度平衡发生移动,达到平衡态II的反应速率随时间变化的关系图如右。该反应为 (填“吸热”或“放热”)反应;升高温度,该反应的平衡常数K值 (填“增大”、“减小”或“不变”)
6H2O+5N2。在一定条件下,该反应达到平衡态I后,升高温度平衡发生移动,达到平衡态II的反应速率随时间变化的关系图如右。该反应为 (填“吸热”或“放热”)反应;升高温度,该反应的平衡常数K值 (填“增大”、“减小”或“不变”)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
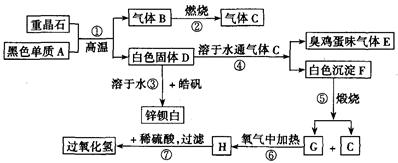
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 红棕色烟,D单质+F单质
红棕色烟,D单质+F单质 黑色固体,A单质+F单质
黑色固体,A单质+F单质 黑色固体。F的最高价钾盐是一种绿色环保型净水剂。
黑色固体。F的最高价钾盐是一种绿色环保型净水剂。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2S和H2SO4 | B.Na2SO3和盐酸 | C.Na2S和盐酸 | D.Na2CO3和H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com